Ежегодно во всем мире выполняется более одного миллиона кардиохирургических операций с искусственным кровообращением (ИК). Одним из наиболее неблагоприятных эффектов ИК является системная воспалительная реакция, лежащая в основе патогенеза таких осложнений, как сердечно-сосудистая, дыхательная, почечная, церебральная, полиорганная недостаточность и пр. [1–3]. Известно, что ряд компонентов анестезии обладает противовоспалительными свойствами [4–8]. Так, экспериментальные и клинические данные свидетельствуют, что опиоидный анальгетик морфин способен значимо угнетать активацию гранулоцитов и макрофагов с последующим нарушением фагоцитоза и падением цитокинов — интерлейкинов 6 и 8 (ИЛ-6, ИЛ-8) [9], фактора некроза опухоли (ФНО) [10]. Сегодня полагают, что данные качества морфина реализуются через влияние на морфин-селективные μ3-рецепторы моноцитов и гранулоцитов [6]. В 2007 году G.S. Murphy et al. показали снижение уровней интерлейкинов, подавление синтеза адгезивных молекул и снижение частоты послеоперационной гипертермической реакции после кардиохирургических вмешательств с ИК при использовании в общей многокомпонентной анестезии морфина [4]. В одном из исследований выявлена более пролонгированная послеоперационная анальгезия при применении морфина [11], что предполагает иммунорегуляторное влияние этого препарата [12].
В свою очередь, другой компонент анестезии — внутривенный гипнотик пропофол в экспериментальных работах также продемонстрировал ряд противовоспалительных свойств [13–18]. На клеточном уровне пропофол ингибирует перекисное окисление липидов, увеличивает высвобождение эндотелием оксида азота, защищает эндотелий от повреждающего действия свободных радикалов, снижая реперфузионные повреждения [14, 19, 20]. К. Mikawa et al. показали, что пропофол в клинических дозировках может подавлять хемотаксис нейтрофилов, фагоцитоз и образование свободных радикалов [21].
Мы не нашли в доступных источниках литературы сведений об исследованиях, посвященных использованию комбинации пропофола и морфина в кардиохирургии, что подчеркивает актуальность научного поиска в данном направлении.
Указанные выше обстоятельства позволили нам сформулировать гипотезу о возможности снижения проявлений СВО в периоперационном периоде кардиохирургических вмешательств при использовании анестезии на основе пропофола и морфина. Для изучения этой гипотезы было проведено клиническое исследование, имевшее следующую цель: оценить влияние различных компонентов анестезии на проявления системного воспалительного ответа в периоперационном периоде кардиохирургических вмешательств, выполненных в условиях искусственного кровообращения.
Одноцентровое проспективное рандомизированное клиническое исследование влияния наркотических анальгетиков и анестетиков на проявления системного воспалительного ответа во время кардиохирургических вмешательств в условиях искусственного кровообращения было выполнено в ФГБУ «Астраханский федеральный центр сердечно-сосудистой хирургии» Министерства здравоохранения РФ в период с сентября 2013 г. по июнь 2016 г. Протокол исследования был одобрен этическим комитетом ФГБУ ФЦССХ.
Мы определили следующие критерии включения в исследование: наличие подписанного пациентом информированного согласия, возраст от 18 до 70 лет, планируемое аортокоронарное шунтирование в условиях ИК. Критериями невключения были: повторные кардиохирургические операции, фракция изгнания левых камер сердца (ФИ) < 30 %, хроническая болезнь почек (креатинин крови > 130 мкмоль/л), легочная гипертензия > I ст. по результату исходной трансторакальной эхокардиоскопии (ЭхоКГ), аллергия на препараты, используемые для анестезии (фентанил, морфин, пропофол, севофлуран), инфаркт миокарда или нестабильная стенокардия в течение 1 мес. до вмешательства, инфекционные и аутоиммунные заболевания в стадии обострения, прием глюкокортикостероидов в предоперационном периоде.
Больные, соответствующие указанным выше критериям, были рандомизированы в два этапа. Первым этапом рандомизации определялся наркотический анальгетик фентанил или морфин, вторым этапом — используемый анестетик пропофол или севофлуран. Таким образом, после выполнения двух этапов рандомизации были сформированы четыре группы. Пациентам 1-й группы проводили анестезию с использованием севофлурана и фентанила, пациентам 2-й группы — севофлурана и морфина, пациентам 3-й группы — пропофола и фентанила, пациентам 4-й группы — анестезию с применением пропофола и морфина.
Премедикация включала прием 0,02 мг/кг феназепама за 12 ч и 1 ч до операции. Интраоперационный мониторинг включал электрокардиографию (ЭКГ), пульсоксиметрию, измерение центрального венозного давления (ЦВД), инвазивного артериального давления (АД), термометрию. Индукция анестезии во всех группах проводилась с применением пропофола (1–2 мг/кг), ардуана (0,07−0,1 мг/кг), морфина в дозе 0,1−0,2 мг/ кг (2-я и 4-я группы) либо фентанила в дозе 5 мкг/ кг (1-я и 3-я группы). В состоянии седации выполняли катетеризацию правой внутренней яремной вены и устанавливали датчик для чреспищеводной ЭхоКГ. Далее по результату рандомизации осуществляли анестезию с использованием севофлурана в дозе 1,5–2 об. % (1-я и 2-я группы) либо инфузии пропофола в дозе 4 мг/кг/ч (3-я и 4-я группы), а также инфузию морфина (0,1 мг/кг/ч во 2-й и 4-й группах) либо фентанила (2 мкг/кг/ч в 1-й и 3-й группах) до окончания операции.
Всем пациентам после стерно- и перикардиотомии выполняли подключение аппарата ИК посредством центральной канюляции восходящей аорты и правого предсердия. До начала ИК после введения 300 ЕД/кг гепарина достигался безопасный уровень антикоагуляции с активированным временем свертывания крови более 450 с. ИК проводили в непульсирующем режиме. Во время ИК продолжали ингаляцию севофлурана в оксигенатор в дозе 0,7–1,5 МАК (1-я и 2-я группы) либо инфузией пропофола в дозировке 4 мг/кг/ч (3-я и 4-я группы) и введением пипекурония (0,05 мг/кг). Целевое артериальное давление в течение ИК было принято в пределах 60−75 мм рт. ст., перфузионный индекс поддерживался в диапазоне 2,4–2,6 л/мин/м². Процедуры ИК проводились в условиях нормотермии. Перфузат для заполнения экстракорпорального контура аппарата ИК содержал: кристаллоидный раствор, коллоидный раствор на основе модифицированного желатина, маннит 15 %, натрия гидрокарбонат, калия хлорид и гепарин. При снижении уровня гемоглобина проводили трансфузию донорских эритроцитов. Аортокоронарное шунтирование выполнялось без кардиоплегии, на работающем сердце, во время параллельной процедуры ИК.
Во всех группах оценивали первичные конечные точки: содержание цитокинов (ИЛ-6, ИЛ-8, ФНО) до ИК, через 1, 3 и 24 ч после прекращения ИК, уровень лейкоцитов на 1-е и 3-и сутки, температуру тела через каждые 2 ч первых суток нахождения в отделении реанимации (ОРИТ).
Для определения системных и иммунологических маркеров воспаления (ИЛ-6, ИЛ-8, ФНО-α) использовались наборы фирмы BIOSOURCE (США), Bender MS (Швейцария). Исследования проводились методом иммуноферментного анализа в соответствии с рекомендациями производителя на электрохемилюминесцентном анализаторе Elecsys-2010 (Roche, Швейцария) в ФЦ г. Астрахани.
К вторичным конечным точкам отнесли: продолжительность искусственной вентиляции легких (ИВЛ), срок лечения в ОРИТ и стационаре, характеристики инотропной и вазопрессорной терапии, осложнения послеоперационного периода и летальность.
Статистического анализ полученного материала в исследованных группах проводился с помощью программы IBM SPSS Statistics (version 2.0). Размер выборки определен с помощью гипотезы о том, что в группе пропофола и морфина уровень интерлейкинов окажется на 20 % ниже, чем в контрольной группе, и предварительного анализа (2 группы по 10 случаев), показавшего, что для определения статистически значимой разницы при мощности 80 %, α = 0,05 и стандартном отклонении 97 размер выборки должен быть равен 27. В связи с этим для данного исследования достаточным количеством для проведения анализа является 30 случаев.
Описательная статистика количественных признаков представлена в виде медианы Ме (25-й; 75-й процентиль) при ненормальном распределении и как среднее и стандартное отклонение (М ± SD) при нормальном распределении.
При нормальном распределении данных применялся дисперсионный анализ. В случае выявления ненормального распределения данных использовали непараметрический критерий Н Краскела—Уоллиса, а для апостериорных сравнений применяли тест U Манна—Уитни. Качественные признаки сравнивали c использованием теста χ2. При множественных сравнениях использовалась поправка Бонферони. Критический уровень значимости нулевой статистической гипотезы об отсутствии различий между группами был принят равным 0,05.
Критериям включения соответствовали 120 пациентов, учитывая отсутствие у этих больных критериев невключения, они были рандомизированы в четыре указанные выше группы по 30 человек в каждой. Один пациент группы 2 (севофлуран–морфин) был выведен из исследования ввиду изменения плана операции — потребовалась пластика митрального клапана.
Клинико-демографические показатели и данные о перенесенных оперативных вмешательствах представлены в табл. 1. Статистически значимых различий по указанным характеристикам между группами обнаружено не было.
| Таблица 1. Клинико-демографические данные пациентов, характеристика выполненных оперативных вмешательств в исследуемых группах (n = 119) | ||||
| Показатель | Группа 1: севофлуран–фентанил, n = 30 |
Группа 2: севофлуран–морфин, n = 29 |
Группа 3: пропофол– фентанил, n = 30 |
Группа 4: пропофол–морфин, n = 30 |
|---|---|---|---|---|
| Пол, муж., % | 65 % | 70 % | 67 % | 72 % |
| Возраст* | 62 ± 10 | 56 ± 8 | 59 ± 7 | 59 ± 6 |
| ИМТ, кг/м2* | 30,9 ± 6,2 | 29,8 ± 5,1 | 28,4 ± 4 | 29 ± 3,9 |
| ФИ ЛЖ, %** | 51 (45–58) | 51 (46–59) | 54,5 (50–60) | 54 (49–60) |
| Euro Score II** | 1,67 (1,19–2,09) | 1,45 (0,98–2,01) | 1,34 (0,96–1,87) | 1,68 (1,11–2,49) |
| Продолжительность операции, мин | 177 (165–190) | 160 (150–175) | 157 (145–185) | 170 (145–200) |
| Длительность ИК, мин | 94,5 (81–128) | 89,5 (75–122) | 91 (75–133) | 101 (79–130) |
| Количество шунтов | 3 (2–3) | 3 (2–3) | 3 (3–4) | 3 (3–4) |
*Данные представлены как среднее ± стандартное отклонение.
**Данные представлены как медиана (интерквартильный размах).
ИМТ — индекс массы тела; ФИ ЛЖ — фракция изгнания левого желудочка.
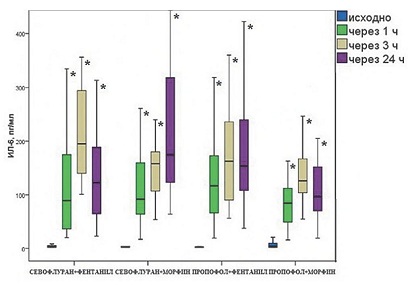
У пациентов всех групп выявлено повышение значений интерлейкинов, что свидетельствует о развитии системной воспалительной реакции после перенесенного ИК. Уровень цитокинов максимально повышался к 1-му или 3-му часу после прекращения ИК и постепенно снижался к концу 1-х сут. Концентрации ИЛ-6, ИЛ-8 и ФНО, определенные после окончания ИК во всех группах, статистически значимо превышали исходные показатели (р < 0,001).
В ходе исследования было выявлено, что в группе 4 (применение морфина и пропофола) рост активности цитокинов был выражен в наименьшей степени, чем в других группах.
Данные, представленные на рис. 1–3, демонстрируют отчетливую тенденцию к определению наименьших концентраций цитокинов в группе 4 (пропофол–морфин). Статистическое подтверждение этот факт получил при сравнении группы 4 (пропофол–морфин) с группой 1 (севофлуран–фентанил) по концентрации ИЛ-6 в точках 3 и 24 ч, ИЛ-8 в точке 1 ч и ФНО в точках 1 и 3 ч. Кроме того, мы обнаружили значимое различие в концентрации ИЛ-6 между группами 4 (пропофол–морфин) и 3 (пропофол-фентанил) в точке 3 ч. Других статистически значимых различий в концентрации цитокинов между изучаемыми группами обнаружено не было.

Рис. 1. Динамика концентрации интерлейкина-6 (ИЛ-6) в плазме крови у пациентов исследуемых групп *p < 0,05 в сравнении с исходными значениями.

Рис. 2. Динамика концентрации интерлейкина-8 (ИЛ-8) в плазме крови у пациентов исследуемых групп *p < 0,05 в сравнении с исходными значениями.
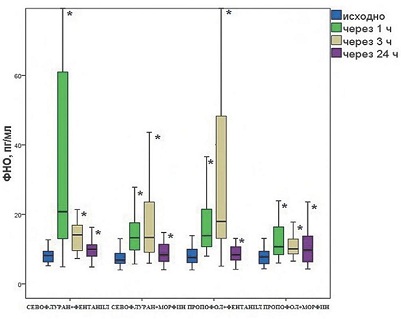
Рис. 3. Динамика концентрации фактора некроза опухоли (ФНО) в плазме крови у пациентов исследуемых групп *p < 0,05 в сравнении с исходными значениями.
Меньшая выраженность системного воспалительного ответа при использовании анестезии на основе пропофола и морфина была подтверждена сниженными показателями кожной температуры через 4 ч после операции: 36,4 (36,1–37) °С в группе 4 (пропофол–морфин) vs 37 (36,7–37,4) °С в группе 1 (севофлуран–фентанил), p = 0,005. Дополнительно сниженный системный воспалительный ответ проявлялся меньшей выраженностью лейкоцитоза. Так, на третьи послеоперационные сутки в группе 4 (пропофол–морфин) этот показатель составил 8,2 (7– 11,4) × 109/л vs 11,1 (9–12,6) × 109/л в группе 1 (севофлуран–фентанил), р = 0,005 (табл. 2).
| Таблица 2. Показатели клинического течения послеоперационного периода в исследуемых группах, медиана (интерквартильный размах) | ||||
| Показатель | Группа 1: севофлуран–фентанил, n = 30 |
Группа 2: севофлуран–морфин, n = 29 |
Группа 3: пропофол–фентанил, n = 30 |
Группа 4: пропофол–морфин, n = 30 |
|---|---|---|---|---|
| Продолжительность ИВЛ, мин | 403 (240–600) | 383 (285–570) | 420 (300–657) | 523 (360–675) |
| Продолжительность пребывания в ОАРИТ, ч | 44 (23–71) | 25,5 (20–73) | 25,2 (19–81) | 24 (21–29)* |
| Продолжительность пребывания в стационаре, ч | 273 (212–322) | 254 (215–309) | 275 (216–321) | 240 (214–288) |
| Частота использования симпатомиметиков, % | 46,7 | 36,7 | 36,7 | 13,3* |
| Частота использования инотропных препаратов, % | 20 | 10 | 10 | 3,3 |
| Частота использования вазоактивных препаратов, % | 43,3 | 33,3 | 33,3 | 10* |
| Температура тела через 4 ч, °С | 37 (36,7–37,4) | 36,9 (36,5–37,4) | 36,7 (36,3–37,3) | 36,4 (36,1–37)** |
| Количество лейкоцитов на 3-и сутки, × 109/л | 11,1 (9–12,6) | 9,5 (7,9–10,5) | 11,2 (8,3–12,3) | 8,2 (7–11,4)** |
*p < 0,05.
**p < 0,01 при сравнении с группой 1 (севофлуран–фентанил).
ИВЛ — искусственная вентиляция легких; ИК — искусственное кровообращение; ОАР — отделение анестезиологии и реанимации.
Значимые различия между исследуемыми группами были обнаружены и в показателях клинического течения послеоперационного периода (табл. 3). Так, время пребывания в ОРИТ было наименьшим в группе 4 (пропофол–морфин) — 24 (21–29) ч, и наибольшим в группе 1 (севофлуран–фентанил) — 44 (23–71) ч, при этом различия между этими группами достигли критического уровня значимости (р = 0,013). Общая частота использования симпатомиметиков была существенно ниже в группе 4 (пропофол–морфин), инфузия этих препаратов потребовалась лишь в 13,3 %, тогда как в группе 1 (севофлуран–фентанил) потребность в симпатомиметиках составила 46,7 %, различия между группами также достигли критического уровня значимости (р = 0,022).
Наше исследование показало значимое повышение концентрации интерлейкинов, наблюдаемое во всех исследуемых группах после завершения искусственного кровообращения, свидетельствующее о развитии системного воспалительного ответа [3, 22, 23]. В соответствии с современными представлениями причинами развития СВО являются такие факторы, как массивная хирургическая травма, активация лейкоцитов и тромбоцитов контуром аппарата ИК, ишемически-реперфузионные повреждения, эндотоксинемия и др. [24].
Нами было выявлено, что, несмотря на одинаковые факторы, способствующие проявлению СВО (объем операции, длительность ИК и операции и пр.), в группе комбинации пропофола и морфина концентрации ФНО, ИЛ-6 и ИЛ-8 были достоверно ниже, чем в группах использования севофлурана и фентанила либо пропофола и фентанила. Кроме того, при комбинации пропофола и морфина были менее выражены температурная реакция и лейкоцитоз, реже использовались симпатомиметики и был короче срок пребывания в ОРИТ.
Одновременное наличие указанных клинических и биохимических различий между исследуемыми группами подтверждает противовоспалительные свойства комбинации пропофола и морфина. Подобные свойства пропофола связывают с его влиянием на функцию макрофагов, проявляющимся подавлением их миграции, фагоцитоза и окислительной способности [25].
H. Chang et al. показали, что пропофол может защищать макрофаги от повреждения, индуцированного оксидом азота [26]. Антиоксидантные свойства пропофола объясняются фенольной структурой, схожей со структурой витамина Е [27]. Эти свойства проявляются ограничением окислительного повреждения, что связывают с реакцией пропофола с токсичными нитроксильными радикалами с трансформацией последних в менее токсичные феноксильные соединения [28] либо со способностью к детоксикации гидроксильных радикалов и предотвращению перекисного окисления липидов [29]. Исследование A. Samir et al. подтверждает наличие у пропофола противовоспалительных свойств, проявляющихся в меньшей концентрации интерлейкинов (ИЛ-6, ИЛ-8), определяемой после ИК [8].
В свою очередь, ряд авторов указывает на противовоспалительные свойства морфина, которые проявляются в снижении выброса медиаторов воспаления и подавлении функции иммунокомпетентных клеток. Экспериментальные данные показывают, что морфин способен угнетать такие функции иммунных клеток, как фагоцитоз, хемотаксис, окислительная активность, а также возможность реагировать на воздействие медиаторов воспаления моноцитами и гранулоцитами [6, 30]. Подобные свойства морфина связывают с его влиянием на морфин-селективные µ3-рецепторы, которые найдены на поверхности различных видов лейкоцитов и иммунокомпетентных клеток [6].
Наличие одновременно противовоспалительных свойств у двух компонентов анестезии — гипнотика пропофола и анальгетика морфина — делает их комбинацию потенциально эффективной. Наше исследование продемонстрировало безопасность подобной комбинации, что подтверждается отсутствием различий во времени ИВЛ, параметрах гемодинамики и частоте развития осложнений. Нам неизвестны другие подобные работы, посвященные использованию комбинации пропофола с морфином с целью снижения проявления СВО, что делает дальнейшие исследования в данном направлении актуальными.
В данном исследовании не определялась концентрация в крови компонентов анестезии для более глубокого изучения иммуномодулирующих свойств данных агентов. Изучали экспрессию ограниченного числа интерлейкинов (ИЛ-6, ИЛ-8, ФНО), не оценивали концентрацию других медиаторов воспаления. В исследование были включены стабильные пациенты невысокого риска. Для дальнейшего подтверждения полученных результатов требуются исследования с большим числом включенных пациентов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов. Аджигалиев Р.Р., Баутин А.Е. — разработка концепции исследования, получение и анализ фактических данных, статистическая обработка, написание и редактирование текста статьи, проверка и утверждение текста статьи; Пасюга В.В. — разработка концепции исследования, получение и анализ фактических данных, написание и редактирование текста статьи, проверка и утверждение текста статьи.
Источники финансирования. ФГБУ «Федеральный центр сердечно-сосудистой хирургии» Минздрава Российской Федерации (г. Астрахань); частное лицо (Аджигалиев Р.Р.).