Нарушение гомеостаза железа является основной стратегией взаимодействия хозяина и патогена. Области научного интереса колеблются от лучшего понимания молекулярных механизмов, лежащих в основе функции метаболизма железа, до потенциальной неблагоприятной роли железа, которая может быть сыграна при ряде критических состояний.
Поэтому современный обзор гомеостаза железа был бы неполным без рассмотрения влияния железа на микробиом и на сепсис, так как большинство бактерий требуют железа для роста и выживания, при этом для некоторых бактерий характерна абсолютная потребность в железе. В настоящем обзоре представлены доказательства автокаталитического участия железа, ведущего, в частности, к манифестации сепсиса. Этот факт ставит ряд вопросов, которые возникают перед клиницистом в период лечения пациентов с сепсисом, где для коррекции анемии часто используют препараты железа и переливание крови. Конечно, точные молекулярные механизмы, каскады и сети, задействованные в метаболизме железа, зависят и от многих других факторов, но тем не менее существуют обширные доказательства участия железа в развитии сепсиса, которые очень трудно игнорировать.
Ценность железа для организма можно объяснить тем, что его метаболизм до минимума исключает потери, а количество всасываемого микроэлемента, напротив, строго лимитировано [1, 2]. Организм человека содержит 3–5 г железа, большая часть которого внутриклеточная, и 65–75 % железа организма связано с порфириновым гемом (в виде гемоглобина) в эритроцитах. Каждый эритроцит может содержать до 280 млн молекул гемоглобина, в результате чего емкость железа составляет более 1 млрд атомов на клетку. Гемоглобин в стареющих эритроцитах тщательно перерабатывается макрофагами в ретикулоэндотелиальной системе, а гемоксигеназа (HO-1) высвобождает железо и монооксид углерода из протопорфиринового кольца, что приводит к образованию биливердина и перемещению железа обратно, в бассейны деятельности трансферрина или ферритина [3].
Сложная система транспортеров регулирует гомеостаз железа у человека, который поддерживается за счет тщательной координации дуоденальной абсорбции и утилизации запасов железа. Баланс железа жестко регулируется для предотвращения пагубных последствий не столько его дефицита, сколько перегрузки железом [4, 5].
На клеточном уровне регуляторные молекулы, такие как ферропортин и гепсидин, вносят вклад в регуляцию железа. Гепсидин — это «антибактериальный» пептидный гормон, вырабатываемый главным образом в печени, и его синтез жестко контролируется на транскрипционном уровне в ответ на уровень поступающего железа, потребности для эритропоэза, и особенно при воспалении или гипоксии [6]. Гепсидин регулирует доступность железа для использования в гемоглобине [7], но может подавлять экспорт железа на уровне тканей, и, наоборот, в ответ на дефицит железа организм может синтезировать дополнительные белковые субстанции для увеличения всасывания и транспортировки железа к местам его потребления [8]. Увеличение общего объема запасов железа в организме запускает выработку гепсидина, который впоследствии вызывает интернализацию и деградацию ферропортина. Поскольку ферропортин присутствует на поверхности макрофагов, гепсидин также уменьшает экспорт железа после рециркуляции ретикулоэндотелиальной системой [9].
Природа включает все механизмы безопасности, так как «знает» железо с «плохой стороны»: как активатора свободно-радикального окисления (СРО) [10], источник энергетического потенциала для бактерий и мембраноагрессора [11–13]. Например, инкубирование эритроцитов от здоровых доноров с плазмой крови больных с септическим шоком индуцировало гидролиз фосфатидилхолина мембраны эритроцитов до лизофосфатидилхолина, что повышало экспрессию фосфатидилсерина эритроцитов [13] и сокращало продолжительность жизни эритроцитов.
Железо является важнейшим микроэлементом не только для людей, но и для бактерий, вирусов, грибков [14, 15]. Внеклеточное и несвязанное железо быстро извлекается трансферрином, ферритином, лактоферрином и другими железопротеинами только с целью безопасности — ограничить доступ железа для бактерий. При воспалении, и тем более при развитии генерализации процесса, у человека повышается синтез ферритина и лактоферрина, в результате возникает «железное голодание» для микробов, ограничивающее их рост, позволяя хозяину вовремя искоренить инфекцию с помощью иммунных механизмов, и конечно, антибиотиков [4, 14–16]. Условия «условной стерильности» тканей жестко привязаны к железу. Для роста бактериальных клеток требуется концентрации железа в среде от 0,4 до 4 мкмолей. Константа же связывания железа трансферрином составляет 1030, а количество свободного железа в равновесии с трансферрином составляет 6 × 10–9мкмолей, что в 108 раз меньше, чем требуется для роста бактерий [17].
Таким образом, во время сепсиса организм использует природную, эволюционно разработанную способность поглощать меньше железа, чтобы лишить вторгающиеся бактерии доступа к железу, которое им необходимо для роста и размножения [14, 17, 18]. Это врожденный иммунный механизм против вторжения патогенов, характерный не только для сепсиса, но и для различных критических состояний [19, 20].
Какие же стратегии используют патогены человека для преодоления всех многочисленных защитных барьеров, созданных природой, чтобы уберечь организм от развития инфекционного процесса и манифестации сепсиса?
Патогены развили сложные стратегии, чтобы обойти «питательный иммунитет» хозяина. Существует несколько механизмов, с помощью которых бактерии реагируют на изменения концентраций Fe в окружающей среде. Самый общий механизм — через отрегулированное выражение системы поглощения железа, включает в себя регулятор поглощения железа (Fur), и небольшие РНК [21–23]. В связи с этим Fur служат в качестве датчиков, которые регулируют факторы вирулентности в дополнение к системам получения железа. Попав в организм хозяина и оценив Fe-окружающую среду, S. aureus реализует много факторов вирулентности, но наиболее активен альфа-токсин (Hla), который и приводит к гемолизу эритроцитов [24, 25].
Для того чтобы высвободить гемоглобин из эритроцитов, многие бактерии выделяют гемолизины. Эти протеины повреждают мембрану эритроцита, приводя к осмотическому лизису, позволяя патогену получить доступ к свободному гемоглобину, и транспортируют эту молекулу в цитоплазму — с целью повредить кольцо гема, для того чтобы получить свободное Fe2+ [26]. В ряде исследований было обнаружено, что S. pneumoniaе уклоняются от «убийства» антибиотиками, нейтрофилами и H2O2 в присутствии эритроцитов человека. Наше собственное исследование показало, что измеренная в первый день течения тяжелого сепсиса концентрация свободного гемоглобина, как следствие гемолиза эритроцитов, выше средней величины и прямо связана с увеличением 30-дневной летальности; уровень свободного гемоглобина в 1-е сутки заболевания характеризуется высокой чувствительностью, специфичностью и с точностью до 96,7 % может определить исход сепсиса [27].
Например, активность P. aeruginosa прямо зависит от приобретения железа у своего хозяина, и во время манифестации сепсиса бактерии могут активно использовать несколько различных систем для сбора железа: с помощью сидерофора пиовердина и путем утилизации гема [28]. Бактерии, используя свои рецепторы внешней мембраны, могут связывать и хелатировать железо непосредственно из трансферрина. Кроме того, бактерии могут синтезировать белки гемофоры, которые способны связывать гем и транспортировать белок хозяина в микробную среду через рецепторное поглощение [29]. Гемофоры, присущие как грамотрицательным (например, Escherichia coli, Pseudomonas aeruginosa, Klebsiella pneumoniae), так и грамположительным бактериям (например, золотистый стафилококк), применяют и второй способ получения железа — путем синтеза и секреции различных сидерофоров [30]. Это приводит к распространению бактерий в периферические органы, при этом активируется секреция провоспалительных цитокинов — интерлейкин-6 (ИЛ-6), нейтрофильные хемоаттрактанты (CXCL1 и CXCL2), которые рекрутируют нейтрофилы в место септического очага, что является демонстрацией неканонической роли сидерофоров в естественных условиях во время клебсиеллезного сепсиса. В дополнение к обеспечению железом возбудителя сидерофоры также способствуют распространению K. pneumoniae в селезенку путем индукции и стабилизации (гипоксия-индуцирующий фактор) HIF-1 в легочных эпителиальных клетках [31, 32].
Таким образом, микроорганизмы, в свою очередь, эволюционировали и приобрели множество стратегий, включая сложные системы транспортеров и регуляторов, для того чтобы получить важный металл, и приобретают железо для своих собственных нужд, как из окружающей среды, так и «похищая» металлы из ресурсов макроорганизма. Для многих типичных грамотрицательных и грамположительных бактерий и патогенных грибов именно гем — самый «богатый» источник железа [33].
Сепсис представляет собой системный иммунный ответ на инфекцию. На сегодняшний день специфического лечения сепсиса пока нет. В настоящее время большое количество публикаций по тематике «обмен железа и сепсис» касается решения вопроса о целесообразности назначения таким пациентам препаратов железа или проведения гемотрансфузии, так как все пациенты с сепсисом имеют анемию воспаления. Как отмечено выше, рост бактерий, вирусов и грибков прямо зависит от наличия железа [34]. Как только насыщение трансферрина в организме человека превышает критический порог, свободное железо сразу становится доступным для использования бактериями [35].
В ряде исследований отмечено, что содержание гепсидина, эритропоэтина и ИЛ-6 в плазме крови больных сепсисом при поступлении в ОРИТ было достоверно выше (при р < 0,05), чем у здоровых добровольцев, и постепенно снижалось на протяжении всего исследования, но на 7-е сутки оставалось достоверно выше (при р < 0,05), чем у здоровых. Плазменный ферритин и (sTfR) трансферриновый рецептор, как и объем эритроцитов на 3-и и 7-е сутки поступления в ОРИТ, были достоверно повышены по сравнению с таковыми у здоровых добровольцев. Кроме того, уровень ферритина плазмы был выше в 3-и и 7-е сутки, чем в 1-е сутки. При прогнозировании 28-дневной летальности плазменный гепсидин имел площадь под кривой 0,808 и специфичность 87,3 %, что было самым высоким показателем среди всех исследуемых параметров, ассоциированных с воспалительной анемией у пациентов с сепсисом [36].
У пациентов с сепсисом, поступающих в ОРИТ, по мнению ряда авторов, быстро развивается анемия, что подтвердили другие исследования [37–39]. Анемия воспаления часто встречается у пациентов с сепсисом в условиях ОРИТ, что подтверждается снижением уровня гемоглобина вместе с изменениями параметров, связанных с анемией воспаления. Однако диагностировать дефицит железа в контексте анемии воспаления очень трудно, главным образом потому, что не существует общепринятого «золотого стандарта» для диагностики дефицита железа в контексте воспаления [40]. Кроме того, традиционные переменные, такие как sTfR и ферритин плазмы, не являются точными для диагностики дефицита железа у пациентов с сепсисом и, по мнению некоторых авторов, даже могут иметь противоположные изменения при железодефицитной анемии без воспаления [41, 42].
В литературе отмечено, что эритропоэз сильно страдает от воспаления, и воспалительные ассоциированные аномалии в эритропоэзе способствуют ранней анемии, выявленной у пациентов с септическим шоком [43]. Эритропоэз строго регулируется эритропоэтином [44], который индуцирует выработку эритроферрона (гликопротеинового гормона, секретируемого эритробластами) и подавляет синтез гепсидина, а значит, облегчает доставку железа во время стрессового эритропоэза [45]. Но оказалось, что воспаление само по себе может ингибировать эритропоэтические эффекты эритропоэтина. Кроме того, эритропоэтин плазмы обычно увеличивается в ответ на анемию и гипоксемию. Однако плазменный эритропоэтин оказался не столь высоким, как ожидалось, и, по данным некоторых авторов, быстро снижался. Это может быть связано с сочетанием нарушения функции почек (что снижает продукцию эритропоэтина) и ингибированием продукции эритропоэтина провоспалительными цитокинами у пациентов с сепсисом [46, 47].
По данным F. Tacke (2016), дисбаланс в метаболизме железа быстро возникает после поступления в ОРИТ наряду с воспалительным процессом, о чем свидетельствует снижение содержания железа и повышение ферритина, уровня sTfR гепсидина и ИЛ-6 в плазме в первую неделю после поступления в ОРИТ [38]. Однако влияние низкого содержания железа в плазме крови на пациентов с сепсисом представляется противоречивым.
С одной стороны, низкий уровень железа может оказывать защитное действие [38], так как железо является незаменимым микронутриентом практически для всех микроорганизмов и, следовательно, низкий уровень железа ограничивает «вредность» микроорганизмов для пациента. Свободное железо токсично, поскольку оно приводит к образованию активных форм кислорода, перекисному окислению липидов и повреждению эндотелия. Кроме того, содержание железа в макрофагах регулирует продукцию ими цитокинов [48, 49].
С другой стороны, слишком низкий уровень железа может привести к низкой доступности железа и железодефицитной анемии и, таким образом, ассоциироваться с неблагоприятными исходами у пациентов с сепсисом [41]. Таким образом, противоречивое влияние низкого уровня железа может объяснить противоречивые результаты (вредные, эффективные или неэффективные), полученные во многих исследованиях по добавкам железа (пероральным или внутривенным) у тяжелобольных пациентов [50, 51]. Кроме того, мы должны учитывать сложность механизмов сепсиса, связанных с анемией [52, 53]. Следовательно, некоторые терапевтические стратегии, такие как гемотрансфузии, добавление железа или антагонизм, использование гепсидина, могут не улучшить эту анемию, а наоборот, вызвать серьезные побочные эффекты.
В исследовании F. Tacke et al. (2016) параметры железа в сыворотке крови при поступлении коррелировали с кратковременной и долгосрочной летальностью у пациентов в ОРИТ. Концентрации гепсидина и ферритина были значительно повышены у пациентов по сравнению с донорами крови и самыми высокими — у пациентов с сепсисом. Напротив, уровни сывороточного железа и трансферрина с самыми низкими значениями отмечались у пациентов ОРИТ с сепсисом. Значения гепсидина коррелировали с уровнями ферритина, а сывороточное железо сильно коррелировало с насыщением трансферрина. Была отмечена умеренная корреляция гепсидина, ферритина и трансферрина с показателями воспаления. Все выжившие пациенты демонстрировали более высокие уровни ферритина и более низкое насыщение трансферрина. В анализах выживших имели место низкие уровни железа (отсечка 10,5 мкмоль/мл), низкое насыщение трансферрина (отсечка 55 %), высокие концентрации трансферрина в сыворотке крови (отсечка 1,6 г/л), которые были связаны с кратковременной и долгосрочной выживаемостью [38]. В подгруппе пациентов с сепсисом, имевших низкие уровни железа и насыщение трансферрина, вообще не отмечалось летальных исходов. Авторы делают выводы, что параметры метаболизма железа, в частности насыщение трансферрина, которые отражают доступность железа в сыворотке крови, являются сильными предикторами исхода у пациентов ОРИТ [38]. Эти данные свидетельствуют о том, что сбой в гомеостазе железа с повышенной доступностью железа в сыворотке происходит у пациентов с сепсисом, что требует проведения проспективных клинических испытаний, оценивающих полезность применения хелатообразующей железа при критических заболеваниях и сепсисе [38].
В контексте сепсиса метаболизм железа является важной терапевтической целью по нескольким причинам. Во-первых, железо необходимо патогену. Во-вторых, дисрегуляция обмена железа может привести (и наверно всегда приводит) к анемии. И, в-третьих, железо само по себе за счет своей токсичности может способствовать развитию патологии. Таким образом, для планирования эффективных терапевтических мероприятий необходимо более глубокое понимание метаболизма железа в организме пациента, тем более в критическом состоянии.
Сегодня перспективный подход к лечению сепсиса чаще рассматривается с осознанием того факта, что железо необходимо как для человека, так и для микробов и это имеет большое значение во многих физиологических и биохимических процессах [54]. Поскольку железо активно участвует в бактериальной пролиферации и иммунной дисрегуляции, можно предположить, что ограничение уровня железа хозяина путем применения хелаторов железа будет способствовать ослаблению бактериального роста и улучшению дисрегуляции внутриклеточной иммунной реакции в ответ на сепсис [55].
Хелатирование железа было предложено в качестве потенциальной терапии полибактериального абдоминального сепсиса [56]. Известно, что лечение хелатированием железа способно ослаблять рост бактерий [57]. Предполагается, что различные типы бактерий будут проявлять различия в их чувствительности к хелатированию железа на основе различий в их метаболизме железа [58]. Грамположительные и грамотрицательные бактерии, как известно, обладают различными системами приобретения железа, могущими повлиять на их реакцию к хелатированию. Новые хелаторы железа, которые не действуют как ксеносидерофоры, могут быть эффективными в лишении этих бактерий железа. Это имеет значение для лечения полибактериального сепсиса, эффективность которого может быть усилена, если известна чувствительность к хелатированию железа первичных возбудителей [59].
Поскольку патогены глубоко нуждаются в железе, чтобы выжить, введение хелаторов выглядит правдоподобной стратегией для лечения сепсиса и преодоления растущей устойчивости, развитой патогенами, к доступным лекарственным средствам. В ряде исследований показано, что хелаторы железа повышают эффективность химиотерапевтических средств против Candida albicans, золотистого стафилококка и полимикробного сепсиса [60, 61, 62].
Учитывая потребность хозяина в железе для его собственных метаболических потребностей, одной из важных проблем, связанных с терапией хелатирования железа, является разработка адекватных стратегий, которые могут гарантировать истощение железа для патогена без сопутствующего дефицита железа у хозяина.
С учетом вышесказанного проясняется другая проблема, которая имеет место в условиях сепсиса — развитие анемии. Эта анемия — результат борьбы микро- и макроорганизмов за выживание. Взаимосвязь между запасами железа у пациента с сепсисом (измеряемыми рутинно по уровню сывороточного железа) и инфекцией является сложной и в настоящее время широко обсуждается под эгидой главного вопроса: приводит ли назначение железа к бактериальному росту и есть ли риск прогрессирования инфекции? При этом нельзя забывать о том, что анемия, вызванная дефицитом железа, встречается у тяжелобольных пациентов только в 9 % [63, 64]. Очень часто эта анемия может носить ятрогенный характер, так как количество суточного забора крови у тяжелобольных пациентов колеблется от 23 до 40 мл в сутки [65] и более.
Существующая сегодня практически повсеместная, а у пациентов с сепсисом — в обязательном порядке, железодефицитная анемия является, по всей видимости, следствием эволюционных механизмов адаптации к постоянной инфекционной угрозе на фоне еще «слабых» побед антибактериальной терапии при сепсисе.
Железо является необходимым питательным веществом почти для всех живых организмов, но его нелегко сделать доступным. Хозяева и патогены вступают в борьбу за металл во время инфекции, что приводит к серьезным изменениям в метаболизме железа хозяина. Указанное взаимодействие может приводить к важным патологическим последствиям, в том числе сепсису, анемии. В свою очередь, анемия, как частое осложнение сепсиса, может быть связана с неблагоприятными исходами.
В противовес сказанному другие исследования показали, наоборот, рост заболеваемости и смертности у пациентов, получающих переливание крови [56]. В исследование Р. Lan (2018) был включен 1891 больной с диагнозом «сепсис» по критериям сепсис-3, из которых у 324 был септический шок. После корректировки для смешанных переменных более высокий квартиль железа был связан с увеличением 90-дневной смертности в регрессионном анализе. Более того, при повышении уровня железа в сыворотке крови у больных с сепсисом наблюдалось поэтапное повышение риска 90-дневной смертности. Авторы сделали заключение, что более высокие уровни железа в сыворотке крови независимо связаны с увеличением 90-дневной смертности в этой большой когорте пациентов с сепсисом [56].
В недавнем исследовании К. Kristof et al. (2018) также отмечено, что у пациентов, получавших трансфузию эритроцитов между 28 днями до развития сепсиса и 28 днями после него (n = 302), отмечалась достоверно более высокая 90-дневная летальность (34,1 % vs 19,6 %; p = 0,004, анализ Каплана—Мейера). Эта ассоциация оставалась значимой после корректировки в многофакторном регрессионном анализе (отношение рисков 1,68; 95 %-й доверительный интервал 1,03–2,73; p = 0,035). У пациентов, получавших трансфузии, также наблюдались достоверно более высокие показатели заболеваемости, такие как баллы по шкале SOFA и длительность пребывания в ОРИТ, по сравнению с пациентами без переливаний (n = 133). Авторы делают вывод о том, что анемия и трансфузия ассоциированы с неблагоприятными исходами у пациентов с сепсисом [66].
В метаанализе N. Nielsen et al. (2017), куда были включены 17 исследований, отмечено, что в целом большинство исследований (11 из 17) пришли к следующему выводу: трансфузия в целом не улучшает оксигенацию тканей или микроциркуляцию. Однако межиндивидуальные эффекты были весьма вариабельны, и более тщательный обзор подгрупп, доступных в 9 исследованиях, показал, что пациенты с аномальной оксигенацией тканей или микроциркуляторными показателями до переливания имели улучшение этих показателей с переливанием, независимо от метода оценки [67]. То есть кому-то стало лучше, а кому-то нет. Этот вывод предлагает новую стратегию для будущих исследований в ОРИТ: использование параметров оксигенации тканей/микроциркуляции для определения потребности в трансфузии, а не произвольной оценки концентрации гемоглобина без учета состояния метаболизм железа.
Авторы обзора С. Dupuis et al. (2017) также констатируют, что на сегодняшний день «…данные о переливаниях эритроцитов у пациентов с сепсисом скудны, а высокая гетерогенность пациентов не позволяет сделать окончательные выводы» [68].
Таким образом, данные, представленные в обзоре, позволяют резюмировать, что метаболизм железа должен контролироваться в ОРИТ, и особенно пристально — у пациентов с сепсисом.
Патофизиология расстройств метаболизма железа у пациентов с сепсисом многофакторна. Она включает:
Так что же несет самый большой риск, когда мы должны переливать и когда мы должны воздержаться? Когда мы должны использовать препараты железа? Должны ли мы иметь фиксированные триггеры для переливания, и если да, то одинаковые у всех пациентов или дифференцированные для разных групп пациентов? Действительно, это более сложные решения, чем первоначально представлялось. Пациенты с сепсисом в ОРИТ очень неоднородны и по-разному реагируют на одно и то же вмешательство.
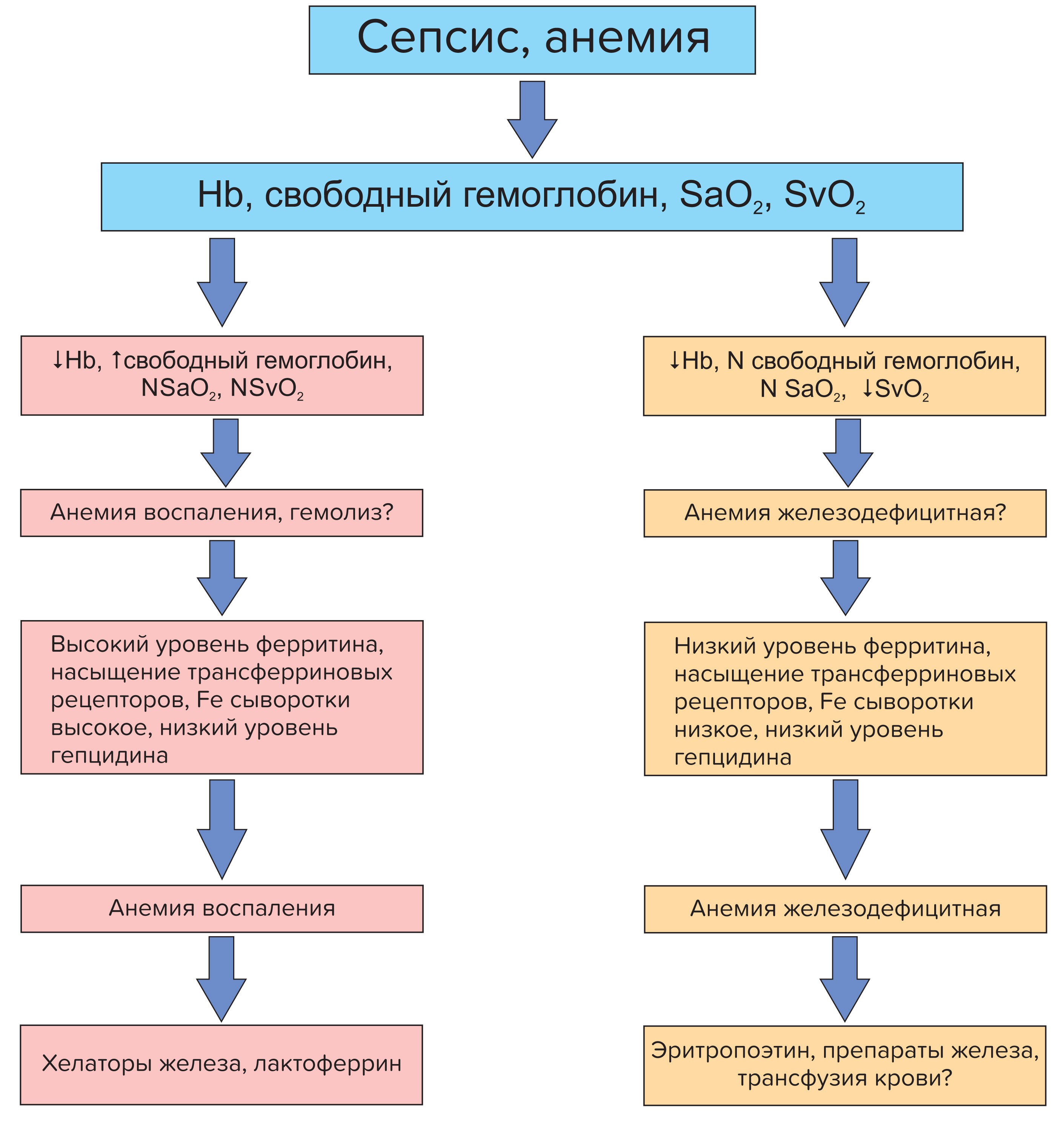
Для решения этого вопроса разумно будет использовать нижеприведенный алгоритм, построенный с учетом данных, представленных в обзоре.

Рис. 1. Алгоритм оценки метаболизма железа у пациента с сепсисом
Как таковые, решения о переливании должны быть строго индивидуализированы с учетом указанных факторов, приведенных в алгоритме, и факторов пациента, таких как возраст и сопутствующие патологии, физиологические переменные, а также значение гемоглобина. Этот подход обеспечит лечение анемии не как симптома, а как гипоксического синдрома (имеющего свои симптомы: снижение Sv, тахипноэ, тахикардию, высокий уровень лактата), когда это необходимо, избегая ненужного использования аллогенных эритроцитов.
Приведенные в обзоре факты являются подтверждением возрастающего интереса к проблеме сепсиса и его связей с железом. Поэтому крайне важно, чтобы фундаментальные исследования продолжали развиваться, с целью более глубокого понимания специфических изменений, происходящих в гомеостазе железа хозяина в ответ на септическую агрессию.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов. Орлов Ю.П. — научное руководство, редактирование статьи; Говорова Н.В., Лукач В.Н., — редактирование статьи; Байтугаева Г.А., Клементьев А.В., Какуля Е.Н. — набор и обработка материала, написание обзора.