
Постепенно, начиная с 60-х гг. XX века, восстановление перфузии миокарда за счет шунтирования коронарных артерий стало рутинной операцией с доказанной эффективностью и положительным влиянием на течение ишемической болезни сердца [1]. В настоящее время операция аортокоронарного шунтирования (АКШ) является самым часто выполняемым в мире кардиохирургическим вмешательством [2]. Внедрение новых технологий сделало проведение операции коронарного шунтирования относительно безопасной процедурой с летальностью, не превышающей 1–2 % [3]. Вместе с тем коронарная хирургия сопровождается высоким риском периоперационных осложнений, обусловленных стернотомией, искусственным кровообращением, сердечной недостаточностью, кровотечением, гемодинамической нестабильностью, послеоперационной дыхательной недостаточностью и другими факторами [3]. Механизм подобных осложнений во многом обусловлен периоперационным стрессом. Так, на фоне повреждения тканей, ишемии-реперфузии и гипоксемии запускается системный воспалительный ответ, который заключается в перестройке метаболизма, развитии инсулинорезистентности и появлении в крови провоспалительных сигнальных молекул [4]. Помимо защитной реакции, такой ответ может носить и негативный характер, приводящий к дополнительному повреждению органов и тканей во время и после оперативного вмешательства.
Приоритетной задачей периоперационного ведения пациентов в различных областях хирургии, направленной на снижение риска и частоты осложнений, является концепция ранней активизации больного (fast-track) [5, 6]. Примерами такого подхода при вмешательствах на сердце, позволяющего уменьшить стрессовый ответ организма на операционную травму, могут служить использование малоинвазивных хирургических технологий (АКШ через миниторакотомный доступ или АКШ на работающем сердце), ранняя мобилизация больного, снижение времени периоперационного голодания, а также мультимодальный подход к анальгезии, включая использование высокой эпидуральной анестезии (рис. 1).

Рис. 1. Способы ослабления хирургического стресса в концепции ранней хирургической реабилитации при аортокоронарном шунтировании
Fig. 1. Methods of abatement surgical stress in the concept of early surgical rehabilitation for coronary artery bypass grafting
Несмотря на использование эпидуральной анестезии и анальгезии в кардиоанестезиологии на протяжении последних 20 лет, на сегодняшний день остаются многочисленные вопросы о целевой группе пациентов для высокой грудной эпидуральной анестезии (ВГЭА), ее достоинствах и недостатках, оптимальной схеме применения методики, дозировках, концентрации и составе лекарств, вводимых в эпидуральное пространство, возможности дополнительного контроля гемодинамических эффектов и ряд других аспектов.
В кардиохирургии широко используется высокий уровень эпидуральной анестезии (Th2–5), обеспечивающий десимпатизацию сердца и устранение чувствительности с этих дерматомов. Учитывая тот факт, что одной из наиболее частых проблем в периоперационном периоде при кардиохирургических вмешательствах являются гемодинамические нарушения, в первую очередь мы рассмотрим влияние эпидуральной анестезии на сердце, а далее клинические последствия применения при коронарном шунтировании.
Как известно, кратковременная регуляция артериального давления обеспечивается двумя рефлексами: барорецепторным и рефлексом Бейнбриджа [7]. Высокая эпидуральная блокада изменяет чувствительность барорефлекса в разных направлениях. Так, в исследовании на добровольцах [8] было показано, что ВГЭА снижает чувствительность барорецепторов в случае повышения давления (прессорного теста), но не меняет их чувствительность при снижении артериального давления (депрессорный тест). При комбинации эпидуральной анестезии с общей анестезией два исследования продемонстрировали схожие результаты в виде уменьшения выраженности ответа частоты сердечных сокращений (ЧСС) на депрессорный тест по сравнению с общей анестезией [9, 10]. Противоположные результаты были получены другими авторами, показавшими у пациентов с эпидуральной анестезией отсутствие различий в реакции ЧСС на артериальную гипотензию, при этом ответ ЧСС был снижен при проведении прессорного теста [11, 12].
Учитывая, что симпатическая нервная система оказывает влияние на свойства миокарда, логично предположить, что десимпатизация будет изменять функционирование миокарда. Исследования, проведенные в отношении систолической функции левого желудочка, показали разнонаправленные результаты; при этом практически все работы по оценке производительности миокарда использовали эхокардиографические параметры. В ряде исследований эпидуральной анестезии было показано улучшение систолической функции сердца, которое проявлялось увеличением сердечного индекса, ударного объема и фракции выброса [13–17]. В некоторых работах с помощью чреспищеводной эхокардиографии была оценена и диастолическая функция миокарда; в большинстве из них выявлено улучшение релаксации левого желудочка на фоне эпидуральной анестезии [15, 18–20]. Тем не менее есть данные о возможном негативном влиянии десимпатизации на миокард. Так, в ряде публикаций было показано ухудшение его систолической функции на фоне эпидурального введения местных анестетиков [14, 21–23]. Вероятно, этот эффект может быть обусловлен фармакологической депрессией миокарда местными анестетиками.
В отношении влияния нейроаксиальной анестезии на функцию правого желудочка объем доступных данных значимо меньше; при этом большинство работ носят экспериментальный характер [24–26]. В целом результаты этих исследований свидетельствуют, что эпидуральная блокада ухудшает систолическую функцию правого желудочка, в частности его геометрическую адаптацию к повышенному давлению в малом круге кровообращения. Результаты клинических публикаций носят противоречивый характер; так, обсервационное исследование, проведенное на 35 больных, выявило улучшение функции правого желудочка после проведения эпидуральной анестезии [27]. Однако данное исследование осуществляли на пациентах, находящихся в сознании, поэтому невозможно экстраполировать его результаты на больных после стернотомии в условиях комбинированной анестезии. Более того, последующая работа этих же авторов при сочетании общей и эпидуральной анестезии показала ухудшение систолической функции правых отделов сердца при использовании эпидуральной анестезии [28].
Тонус сосудистой стенки и системное сосудистое сопротивление в значительной степени регулируются симпатической нервной системой. При введении местного анестетика в эпидуральное пространство происходит блокада импульсов симпатических нервов на уровне соответствующих дерматомов. По данным экспериментальных исследований на животных, эффекты выключения влияния симпатической нервной системы на сосудистый тонус могут варьировать — от отсутствия влияния [29] до значимого снижения сосудистого сопротивления [30, 31]. При исследовании динамики сосудистого сопротивления у пациентов во время кардиохирургических вмешательств с использованием эпидуральной анестезии было показано, что блокада кардиальных дерматомов снижает сосудистое сопротивление [32]. Такой эффект может иметь позитивное значение в виде ослабления гипертензивной реакции в ответ на стернотомию и обеспечения стабильной гемодинамики [33, 34]. Следует отметить, что анальгетический эффект эпидурального введения местных анестетиков и наркотических анальгетиков позволяет уменьшить интраоперационный расход препаратов для анестезии. Так, в нашем исследовании при ВГЭА 0,75 % ропивакаином отмечено снижение дозы пропофола в среднем на 15 %, а фентанила — на 50 % [34]. Тем не менее ВГЭА, особенно при использовании высоких дозировок местных анестетиков, может увеличивать потребность в назначении вазопрессоров [32, 89] и объем инфузионной терапии [34].
Коронарный кровоток также во многом регулируется автономной нервной системой [7]. Несмотря на всю его важность, во многих ситуациях существуют трудности с однозначной оценкой величины миокардиальной перфузии. Исследования, проведенные на животных в различных экспериментальных моделях, выявили, что временное снижение влияния симпатических нервов в дерматомах Th2–5 приводит к коронародилатации и значимому перераспределению кровотока миокарда из эпикардиальных отделов в эндокардиальные, что сопровождается снижением потребления кислорода сердцем [35–38]. При этом в ряде экспериментальных работ был показан положительный эффект эпидуральной анестезии на уменьшение зоны инфаркта миокарда [36, 39].
Исследования коронарного кровотока у пациентов в кардиохирургии продемонстрировали менее однозначные результаты [40]. Тем не менее у пациентов с хронической сердечной недостаточностью торакальная эпидуральная анестезия ассоциировалась с более высоким коронарным кровотоком по сравнению с контрольной группой [41]; работа Bulte и соавт. 2017 г. также показала увеличение миокардиального кровотока [42]. При более углубленном изучении коронарной перфузии с помощью позитронно-эмиссионной томографии и тканевой оксиметрии выявлена корреляция торакальной эпидуральной анестезии с улучшением коронарного кровотока. Так, на фоне эпидуральной анестезии Eygård и соавт. с помощью радионуклидных методик показали улучшение кровотока в стенозированных артериях у пациентов с ишемической болезнью сердца [43], а Lagunilla и соавт. обнаружили повышение парциального давления кислорода в миокарде [44].
Осложнения со стороны дыхательной системы встречаются после 5–25 % кардиохирургических вмешательств; их тяжесть варьирует от транзиторной гипоксемии до тяжелого острого респираторного дистресс-синдрома [45, 46]. Патогенез респираторных осложнений при коронарном шунтировании связан с хирургической травмой, искусственным кровообращением, гемотрансфузией, избыточным гидробалансом, неадекватным купированием болевого синдрома, ателектазированием легких и другими факторами [45, 47]. Высокая торакальная эпидуральная анестезия в кардиохирургии за счет купирования болевого синдрома, десимпатизации, снижения давления и перераспределения жидкости в малом круге кровообращения может способствовать уменьшению выраженности отека и ателектазирования легких, а также снижению частоты дыхательных осложнений [48–54].
Наиболее частой причиной развития периоперационного инфаркта миокарда является нарушение кровотока по ветвям коронарных сосудов, вызванное разрывом атеросклеротической бляшки [55]. В связи с этим во время кардиохирургических вмешательств жизненно необходим контроль факторов, которые позволяют стабилизировать состояние эндотелия и коронарный кровоток. В теории существуют две стратегии, которые заключаются в постоянном медикаментозном контроле стабильности бляшки и в профилактике ее стресс-индуцированного разрыва в периоперационном периоде. В этом плане может быть с успехом использована высокая эпидуральная блокада, позволяющая снизить постнагрузку и уменьшить системное сосудистое сопротивление [56, 57].
Влияние регионарных методик на развитие периоперационного инфаркта при коронарном шунтировании остается предметом дискуссий. Ряд авторов отмечают меньшую частоту послеоперационной ишемии миокарда [14, 58], в то время как в других работах не наблюдали данного благоприятного эффекта [59–63]. Несмотря на это, анализ компилированных данных показывает, что использование высокой эпидуральной блокады в кардиохирургии может снизить риск периоперационного инфаркта миокарда [64, 65]. Это подтверждается и систематическим Кокрейновским обзором 2019 г., в котором показано снижение частоты развития инфаркта миокарда при использовании торакальной анестезии в первые 30 суток после кардиохирургических вмешательств.
Нарушения ритма являются частыми осложнениями послеоперационного периода в коронарной хирургии, среди них превалирует фибрилляция предсердий (от 10 до 50 % всех кардиохирургических вмешательств) [46]. Чаще всего фибрилляция предсердий носит транзиторный характер, вместе с тем она повышает риск развития цереброваскулярных осложнений, желудочковых аритмий, гемодинамической нестабильности и летального исхода, особенно у пациентов со сниженной фракцией выброса [66]. Повышенный симпатический тонус как ответ на боль и операционную травму может повышать электрическую нестабильность миокарда, что потенциально создает предпосылки для благоприятных эффектов десимпатизации в данной клинической ситуации. Вместе с тем узконаправленный метаанализ, объединяющий рандомизированные исследования частоты фибрилляции предсердий в группах пациентов после коронарного шунтирования в условиях традиционной общей анестезии и при ее комбинации с эпидуральной блокадой, не выявил достоверных различий [67]. Противоположный результат был получен другими авторами, которые показали, что применение нейроаксиальной анестезии и общей анестезии ассоциировалось с более низкой частотой развития послеоперационных аритмий [68]. Данные еще одного метаанализа об использовании эпидуральной блокады в кардиохирургии доказывают статистически значимый протективный эффект комбинированной анестезии в отношении аритмий, однако в нем использованы результаты исследований не только при хирургии коронарных сосудов, но и при вмешательствах на клапанах сердца [54].
Тромбоз глубоких вен и тромбоэмболия легочной артерии — опасные осложнения любого крупного хирургического вмешательства. По данным метаанализа Ho и соавт., медианные значения тромбоза вен нижней конечности и симптомной легочной эмболии в кардиохирургии составляют 3,2 и 0,6 % соответственно [69]. В целом ряде исследований показано, что эпидуральная анестезия за счет снижения операционного стресса может уменьшать выраженность гиперкоагуляционного синдрома [70, 71] и частоту тромбоза вен нижней конечности [72, 73]. Вместе с тем, несмотря на снижение коагуляционного потенциала, эпидуральная анестезия в кардиохирургии не увеличивает риск дренажной кровопотери и не повышает частоту гемотрансфузий при сравнении с общей анестезией [70, 74–76], а по данным некоторых работ, даже может способствовать их снижению [61, 77].
Эффективное обезболивание и сокращение длительности послеоперационной вентиляции легких — один из ключевых компонентов ранней реабилитации пациентов после кардиохирургических операций [78]. Такой подход укорачивает время нахождения в отделении интенсивной терапии и снижает экономические издержки [79]. Эпидуральное введение местных анестетиков обеспечивает повышение качества анальгезии в периоперационном периоде АКШ, что подтверждается целым рядом исследований [53, 80, 81]. Кроме того, проведение эпидуральной анальгезии при коронарном шунтировании способствует улучшению артериальной оксигенации и уменьшает длительность искусственной вентиляции легких [50, 53, 82]. Эти эффекты подтверждены в недавнем метаанализе [54] и являются дополнительным доводом для более широкого использования нейроаксиальных методик в кардиохирургии. Как правило, после кардиохирургического вмешательства для эпидуральной анальгезии используется более низкая концентрация анестетика по сравнению с интраоперационным периодом [54]. Так, в нашем исследовании ВГЭА при АКШ на работающем сердце концентрация ропивакаина после вмешательства уменьшалась с 0,75 до 0,2 % [34]. При этом инфузионный способ введения, в том числе в режиме аутоанальгезии, может значимо повышать качество обезболивания [34, 53, 54].
Безопасность и возможность улучшения клинических исходов служат ключевыми требованиями, которые предъявляются к различным методам лечения. В этом плане данные по использованию эпидуральной анестезии в кардиохирургии достаточно противоречивы. Систематические обзоры, посвященные применению эпидуральной анестезии при операциях на сердце в целом и, в частности, в коронарной хирургии, не выявили различий в послеоперационной летальности [54, 64, 65, 83]. Отчасти это может быть обусловлено различными схемами эпидуральной анестезии и анальгезии, использующими, как правило, лидокаин, бупивакаин, левобупивакаин или ропивакаин, в том числе в ряде случаев в сочетании с наркотическими анальгетиками. В частности, в метаанализе Bignami и соавт. [64] лишь в 21 работе из 33 применялись концентрированные растворы местных анестетиков (0,5–1%). Кроме того, большую проблему для исследований составляют многофакторность клинических исходов и относительно низкая летальность после коронарного шунтирования, что требует значимого увеличения количества пациентов для проведения исследований необходимой мощности [84–90].
Одним из опасных осложнений нейроаксиальных методик обезболивания является эпидуральная гематома, частота которой при кардиохирургических вмешательствах может повышаться в связи с необходимостью интраоперационного использования антикоагулянтов, особенно при операциях с искусственным кровообращением [84]. Тем не менее при тщательном соблюдении требований к безопасности процедуры частота технических осложнений регионарных методик в кардиохирургии, в частности развития гематом, связанных с постановкой эпидурального катетера, не превышает таковую в общей популяции, составляя в среднем 1 случай на 6000 анестезий [85]. Эти результаты были подтверждены в метаанализе 2019 г., сравнивавшем частоту осложнений в группах общей и комбинированной анестезии [54]. Следует отметить, что в данный анализ попали пациенты, оперированные как на работающем сердце, так и в условиях искусственного кровообращения. Тем не менее для профилактики эпидуральной гематомы в кардиохирургии важно соблюдать минимальный часовой интервал между постановкой эпидурального катетера и введением гепарина, а при использовании искусственного кровообращения и гепаринизации 300 МЕ/кг ряд авторов рекомендует постановку эпидурального катетера вечером перед операцией [86, 87]. Кроме того, с введением гепарина необходимо синхронизировать и время удаления эпидурального катетера, соблюдая при этом соответствующий интервал [86].
В целом достоинства и недостатки ВГЭА суммированы на рис. 2.
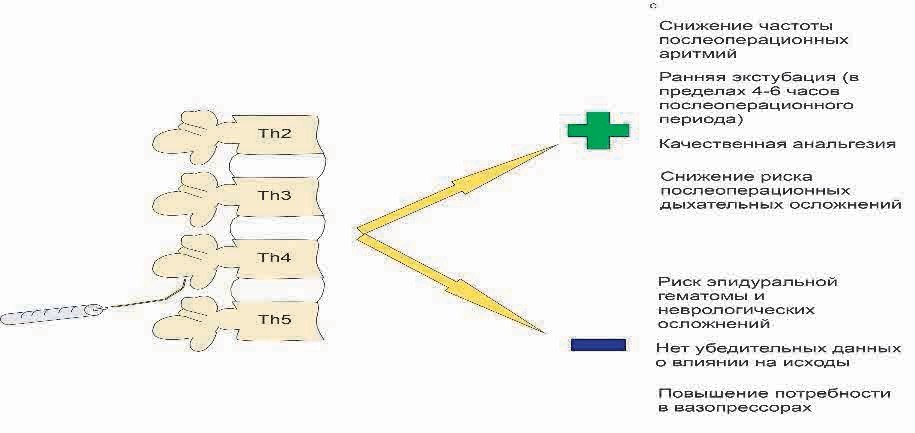
Рис. 2. Преимущества и недостатки эпидуральной анестезии в кардиохирургии
Fig. 2. Advantages and disadvantages of epidural anesthesia in cardiac surgery
Применение высокой эпидуральной блокады в коронарной хирургии позволяет обеспечить адекватное обезболивание пациента и ассоциируется с улучшением качества реабилитации после кардиохирургических операций. Протективные эффекты высокой торакальной эпидуральной анестезии и анальгезии в отношении дыхания и кровообращения могут быть обусловлены не только анальгезией, но и управляемой десимпатизацией, которая приводит к уменьшению метаболического стрессорного ответа на хирургическую травму. По данным исследований и метаанализов последних лет, использование эпидуральной анестезии и анальгезии в кардиохирургии приводит к снижению частоты развития легочных осложнений, сокращению длительности искусственной вентиляции легких и уменьшению частоты развития аритмий, без влияния на частоту летальных исходов. В связи с этим регионарная анестезия может быть важным компонентом анестезиологического пособия, в первую очередь при реваскуляризации миокарда на работающем сердце. Гетерогенность проведенных исследований и противоречивость ряда результатов обусловливают необходимость дальнейшей работы для определения места нейроаксиальных блокад в кардиохирургии.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов. Волков Д.А., Паромов К.В., Еремеев А.В., Киров М.Ю. — разработка концепции статьи, получение и анализ фактических данных, написание и редактирование текста статьи, проверка и утверждение текста статьи.
ORCID авторов
Волков Д.А. — 0000-0003-1558-9391
Паромов К.В. — 0000-0002-5138-3617
Еремеев А.В. — 0000-0002-8537-1163
Киров М.Ю. — 0000-0002-4375-3374