В научной литературе приведено достаточно данных о необходимости поддержания энтерального кормления у пациентов в критическом состоянии [1, 3]. Проблема, связанная с недостаточной толерантностью к энтеральной нагрузке, особенно широко распространена в отделении интенсивной терапии новорожденных [2]. Гастроэзофагеальный рефлюкс является основным клиническим проявлением сниженной толерантности к энтеральному питанию. Американское общество парентерального и энтерального питания рекомендует постпилорическое введение питательных смесей пациентам с высоким риском аспирации и/или при непереносимости кормления при питании через гастральный зонд. По данным литературы, проведение нутритивной поддержки через питательный зонд, установленный за пределы пилорического отдела желудка, продемонстрировало достаточный терапевтический эффект, что в ряде случаев позволяет начать эффективное энтеральное питание, минимизируя количество возможных последствий голодания. При этом размещение питательного зонда за пределы привратника является достаточно сложной и трудоемкой манипуляцией [4]. Успешность установки зонда, по данным литературы, весьма вариабельна, по разным источникам — от 45 до 87 %. Показанием для установки зонда за пилорическим отделом желудка является прежде всего невозможность гастрального кормления: тяжелый желудочно-пищеводный рефлюкс, непереносимость энтерального питания при проведении неинвазивной искусственной вентиляции легких, нарушение моторики и/или парез желудка [1]. Постановка транспилорического зонда, как правило, происходит «вслепую», с последующим рентгенологическим контролем. Известно несколько методов, способствующих эффективному проведению постпилорического питания у детей, но в настоящее время не существует согласованного стандартного протокола постановки питательного зонда и контроля его положения [5]. При этом «неудачное» размещение питательного зонда через пилорический отдел желудка приводит к «излишнему» использованию рентгенографии и задержке начала необходимой нутритивной поддержки. Рентгенография является малоэффективным методом контроля и несет в себе потенциально вредные дозы радиации [6]. Кроме того, недостатком рентгенологического исследования является неточное определение положения конца зонда и невозможность его визуализации в режиме реального времени [7]. Ультразвуковое исследование пилорического отдела желудка является эффективным и безопасным методом наблюдения за положением питательного зонда без необходимости облучения пациента [8].
Цель исследования — повышение эффективности контроля положения питательного зонда.
Исследование проводилось на базе областного государственного автономного учреждения здравоохранения «Городская Ивано-Матренинская детская клиническая больница», г. Иркутск, с июня по ноябрь 2021 г. В исследование были включены 17 пациентов в возрасте от 10 до 90 дней жизни. Все пациенты, включенные в исследование, нуждались в проведении интенсивной терапии и имели низкую толерантность к энтеральной нагрузке при кормлении через гастральный зонд. В исследование не были включены пациенты с врожденными пороками развития и дети после оперативного вмешательства на органах желудочно-кишечного тракта, а также дети с противопоказаниями для энтерального питания. Для проведения процедуры размещения питательного зонда была организована бригада, состоящая из двух врачей-реаниматологов, которые имели достаточные знания и опыт в постановке зондов для энтерального питания. Один из врачей обладал достаточными теоретическими и практическими знаниями в ультразвуковой диагностике и выполнял контрольную функцию. В исследовании были использованы поливинилхлоридные зонды размером 5 Fr или 6 Fr, длиной 50 см. Зонды вводились назогастрально и продвигались до появления сопротивления, с последующим постепенным введением до заранее отмеченной метки. Глубина введения зонда была индивидуальной. При введении зонда через носовой ход необходимая глубина введения питательного зонда включала сумму расстояний: от ноздри до козелка уха, от козелка до средней точки между мечевидным отростком и пупком, от средней точки между мечевидным отростком и пупком до середины реберной дуги (рис. 1). С целью придания зонду упругости использовался металлический проводник с витым мягким кончиком. В исследовании использовался портативный ультразвуковой сканер Mindray М7 (Китай). Пациентов помещали в положение лежа на спине, ультразвуковое сканирование проводилось с использованием линейного трансдьюсера 10–12 МГц. При проведении исследования использовался серошкальный режим (В-режим). Для этой цели датчик позиционировали в субкостальной области, визуализировали антральную часть желудка между печенью и поджелудочной железой, далее лоцировался пилорический канал и постпилорическая область — двенадцатиперстная кишка (рис. 2). После четкой визуализации пилорического канала приступали к процессу установки зонда для энтерального питания. При размещении применялся следующий алгоритм: зонд, установленный назогастрально, плавно продвигался до появления сопротивления. Зонд фиксировался и с последующим интервалом в 5 мин продвигался в среднем на 1 см. После 3–4 манипуляций выполняли исследование пилорического канала, где визуализировали питательный зонд. Далее врач, выполняющий постановку зонда, медленно продвигал его до заранее отмеренной метки. В это время врач, выполнявший ультразвуковой контроль, визуализировал ход зонда по пилорическому каналу. В завершение, чтобы убедиться, что дистальный конец питательного зонда находится в постпилорической области, извлекался проводник и в зонд вводилось 5–10 мл 0,9 % раствора натрия хлорида. Если в просвете двенадцатиперстной кишки появлялось анэхогенное содержимое после введения физиологического раствора, то постановка считалось успешной (рис. 3, 4). После успешной процедуры установки транспилорического зонда его расположение подтверждалось рентгенологически (рис. 5, на данном снимке в зонд был введен рентген контрастный препарат — урографин 0,5 мл для улучшения визуализации зонда). Врачи, описывающие рентгенограммы, не имели информации о результатах ультразвукового исследования. Побочных эффектов во время проведения процедуры у недоношенных детей не было. Статистическая обработка проводилась с использованием метода непараметрического анализа данных. Статистический анализ проводился с использованием программы STATISTICA 13.3. Номинальные данные описывались с указанием абсолютных значений и процентных долей. Количественные данные представлены в виде медианы и квартилей (25–75 % границы интерквартильного отрезка). Сравнение статистических показателей проводилось с помощью критерия χ2 Пирсона. За уровень статистической значимости принято значение р < 0,05. Прогностическая модель, характеризующая зависимость количественной переменной от факторов веса пациентов и времени установки зонда, исследовалась с помощью метода линейной регрессии. Проведение исследования одобрено локальным этическим комитетом ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск (протокол № 10 от 28 ноября 2021 г.). Все законные представители детей добровольно выразили свое согласие на участие в медицинском исследовании.
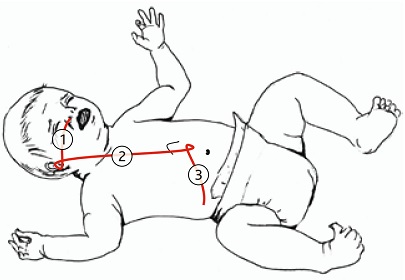
Рис. 1. Определение необходимой глубины введения зонда. При введении транспилорического зонда через носовой ход необходимая глубина введения включает сумму расстояний: 1 — от ноздри до козелка уха; 2 — от козелка до средней точки между мечевидным отростком и пупком; 3 — от средней точки мечевидным отростком и пупком до середины реберной дуги
Fig. 1. Determination of the required depth of insertion of the tube. The required depth of introduction of the transpyloric tube includes three distances: 1 — from the nostril to the tragus of the ear; 2 — from the tragus to the midpoint between the xiphoid process and the navel; 3 — from the midpoint of the xiphoid process and the navel to the middle of the costal arch

Рис. 2. Эхографическая визуализация пилорического отдела желудка: 1 — тело поджелудочной железы; 2 — пилорический канал; 3 — селезеночная вена; 4 — паренхима печени; 5 — желудок
Fig. 2. Echo-graphic visualization of the pyloric part of the stomach: 1 — body of the pancreas; 2 — pyloric canal; 3 — splenic vein; 4 — liver parenchyma; 5 — stomach
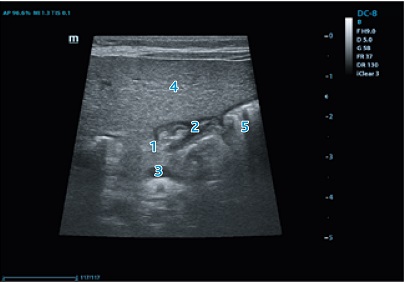
Рис. 3. Продвижение питательного зонда по пилорическому каналу: 1 — тело поджелудочной железы; 2 — пилорический канал; 3 — селезеночная вена; 4 — паренхима печени. Проекция зонда указана стрелкой — виден двойной параллельный контур
Fig. 3. Advancement of the nutrient tube along the pyloric canal 1 — body of the pancreas; 2 — pyloric canal; 3 — splenic vein; 4 — parenchyma of the liver. The projection of the probe is indicated by an arrow — a double parallel contour is visible

Рис. 4. Изменения эхогенности в постпилорической зоне: 1 — тело поджелудочной железы; 2 — пилорический канал с анэхогенным содержимым; 3 — селезеночная вена; 4 — паренхима печени. Проекция зонда указана стрелками — виден двойной параллельный контур
Fig. 4. Changes in echogenicity in the postpyloric zone: 1 — body of the pancreas, 2 — pyloric canal with anechoic contents, 3 — splenic vein, 4 — liver parenchyma. In the picture, the projection of the probe is indicated by arrows — a double parallel contour is visible
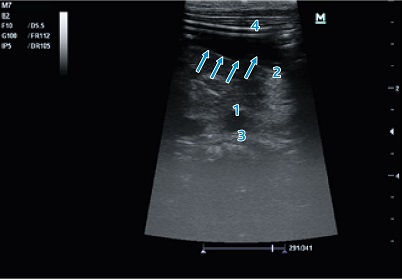
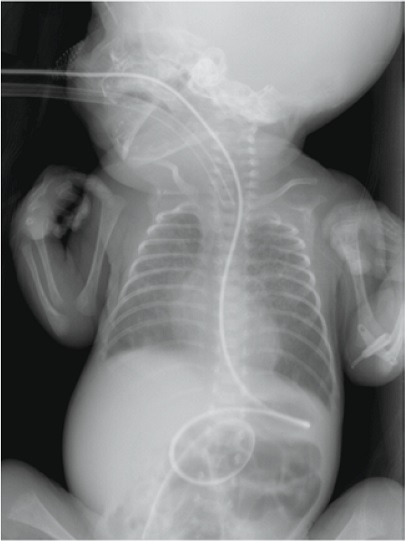
Рис. 5. Обзорная рентгенограмма грудной клетки и живота в прямой проекции. В питательный зонд введен рентгеноконтрастный препарат. На снимке видно, что конец зонда расположен за пределами привратника
Fig. 5. Plain radiograph of the chest and abdominal organs. An X-ray contrast agent was introduced into the tube. The image shows that the end of the probe is located outside the pylorus
При оценке с помощью ультрасонографии, проведенной перед процедурой установки зонда для кормления, пилорический отдел и постпилорическая область были визуализированы у 17 (100 %) пациентов. Возраст пациентов составил от 10 до 90 дней, М — 26 дней; Q1–3 [15–45] дней. Диапазон веса: 0,8–2,6 кг, М — 1,8 кг; Q1–3 [1,3–2,3] кг. Время завершения ультразвукового исследования в среднем составило 19 мин (диапазон 3–30 мин), М — 17 мин; Q1–3 [14–25,5] мин. У 16 пациентов (94,1 %) питательный зонд был визуализирован в пилорическом отделе желудка и двенадцатиперстной кишке. В 10 исследованиях (58,8 %) имело место полное совпадение заключений рентгенологического и ультразвукового исследования. В 7 случаях (41,2 %) рентгенолог не смог определить точное расположение дистального конца зонда между отделом двенадцатиперстной и тощей кишки. У 1 пациента (5,9 %) сонограмма была неправильно интерпретирована, конец зонда был визуализирован в пилорическом канале, в то время как рентгенологически позиция зонда имела иное расположение. В ходе исследования было выявлено статистически значимое различие в верификации ультразвукового контроля постановки зонда в сравнении с рентгенологическим исследованием (р < 0,05). Значение критерия χ2 составило 5,8, а критическое значение χ2 — 3,8 при уровне значимости p = 0,05.
В связи с низкими резервами питательных веществ и более высокими потребностями в энергии и пластических материалах новорожденные более чувствительны к гиперкатаболическим процессам, что требует разработки четкого алгоритма проведения нутритивной поддержки. Понимание необходимости поддержания нутритивной поддержки у недоношенных детей в тяжелом состоянии инициирует максимально раннее ее начало. Ранний переход с парентерального питания к энтеральному кормлению способствует профилактике синдрома транслокации бактериальной флоры «голодной» кишки. Однако многочисленные исследования демонстрируют тот факт, что недоношенные младенцы очень часто неспособны переносить гастральное кормление. Проведенные научные работы по выявлению оптимального метода кормления противоречивы. Большая часть из них показывает, что использование транспилорического кормления сопоставимо по эффективности с оперативной фундопликацией. Использование ультразвукового метода визуализации положения питательного зонда является эффективным и безопасным, он может предотвратить избыточную лучевую нагрузку при проведении рентгенографии. Большинство опубликованных работ применения ультразвукового исследования в постановке питательного зонда проводились у взрослых и детей старше года. В одноцентровом ретроспективном исследовании, проведенном под руководством Итиро Осава, показатель успешности постановки транспилорического зонда в группе с ультразвуковым контролем был выше, чем в группе «слепого» введения. Хотя визуализация привратника с помощью ультразвука относительно проста, установка питательного зонда с ультразвуковой навигацией может быть затруднительна, поскольку мягкий, податливый зонд нелегко провести через пилорический канал. Использование металлического проводника с витым мягким концом облегчает процесс продвижения. Мы пришли к выводу, что использование ультрасонографии при размещении питательного зонда возможно и имеет определенные преимущества по сравнению с обычной рентгенографией. Этот метод контроля с успехом может быть применен в отделениях интенсивной терапии новорожденных и детей, в которых доступен портативный ультразвуковой аппарат.
Обширные исследования показывают, что использование транспилорического кормления сопоставимо по эффективности с оперативной фундопликацией. Постановка питательного зонда за пределами пилорического отдела желудка у тяжелобольных младенцев может привести к улучшению результатов лечения, однако процесс проведения зонда через верхние отделы желудочно-кишечного тракта может быть проблематичным. Полученные данные свидетельствуют, что ультразвуковая визуализация зонда имеет статистически значимые преимущества в сравнении с рентгенологическим контролем. Использование ультразвукового исследования для визуализации процесса установки питательного зонда может исключить дополнительное использование рентгенографии.
Этическое утверждение. Исследование было одобрено локальным этическим комитетом ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск, Россия (протокол № 10 от 28 ноября 2021 г.).
Ethics approval. The present study protocol was approved by the local Ethics Committee of the Russian Medical Academy of Continuous Professional Education, Irkutsk, Russia (reference No 10, 28/11/2021).
Информация о финансировании. Авторы заявляют об отсутствии внешнего финансирования при проведении исследования.
Funding source. This study was not supported by any external sources of funding.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Disclosure. The authors declare that they have no competing interests.
Вклад авторов. Все авторы в равной степени участвовали в разработке концепции статьи, получении и анализе фактических данных, написании и редактировании текста статьи, проверке и утверждении текста статьи.
Author contribution. All authors according to the ICMJE criteria participated in the development of the concept of the article, obtaining and analyzing factual data, writing and editing the text of the article, checking and approving the text of the article.