Ожирение является одной из нарастающих современных медико-социальных и экономических проблем человеческого сообщества. За последние 40 лет отмечается существенное увеличение числа лиц с избыточной массой тела и ожирением [1–3]. G. Singh и соавт., анализируя данные на 2009 г., показали, что во взрослой (≥ 18 лет) популяции США встречаемость лиц с избыточной массой тела увеличилась с 36,9 до 62 %, а с ожирением — с 8,7 до 27,4 % [1]. Рост числа лиц с избыточной массой наблюдается и в Российской Федерации, охватывая в целом по разным регионам до 56 % мужчин и 62 % у женщин [4]. Подтверждает эту тенденцию в России и Всемирная организация здравоохранения: согласно ее данным, на 2009 г. избыточную массу тела либо ожирение имели 46,5 % мужчин и 51,7 % женщин [5]. По данным доклада ООН, в 2013 г. Российская Федерация занимала 19-е место среди всех стран мира по распространенности ожирения [6]. За последние три десятилетия распространенность избыточной массы тела и ожирения в мире выросла почти на 30–50 % среди взрослых и детей. По предварительным оценкам, к 2030 г. 86,3 % взрослого населения планеты будут иметь избыточную массу тела и 51,1 % — ожирение [5]. Избыточная масса тела сегодня предопределяет развитие до 44–57 % всех случаев сахарного диабета 2-го типа, 17–23 % — ишемической болезни сердца, 17 % — артериальной гипертензии, 30 % — желчнокаменной болезни, 14 % — остеоартрита, 11 % — злокачественных новообразований [5–6]. Наряду с консервативным ведением пациентов в последние годы в РФ отмечается повышение интереса к бариатрической хирургии и значительно выросло количество операций, направленных на лечение морбидного ожирения. Среди хирургических операций наибольшую популярность и эффективность приобрели: гастрошунтирование, рукавная резекция желудка и бандажирование желудка (10 %). Эти хирургические вмешательства не только приводят к снижению массы тела, но и нормализуют повышенное артериальное давление, улучшают течение сахарного диабета и функции легких, а также увеличивают отдаленную выживаемость, повышая качество жизни [7]. В настоящее время количество бариатрических операций в России стало составлять около 3000 в год [8]. Между тем известно, что инфекции области хирургического вмешательства при бариатрических операциях широко варьируют и встречаются с частотой от 1 до 21,7 % [9–10]. Большинство специалистов полагают, что в этой ситуации целесообразно придерживаться тактики традиционной периоперационной антибиотикопрофилактики, принимая во внимание особенности этиологии инфекций области хирургического вмешательства в бариатрии и фармакокинетики препарата [11–13]. Между тем частота инфекции области хирургического вмешательства менее 5 % коррелирует с ее побочными эффектами и заставляет задуматься о ее необходимости. Новому витку актуализации проблемы способствовал переход на эндовидеохирургические технологии оперирования, когда стало очевидным, что при использовании эндоскопической техники инфекции области хирургического вмешательства встречаются значительно реже [14–15]. Роль непосредственно периоперационной антибиотикопрофилактики при доминировании эндоскопических технологий и невысокой в целом встречаемости инфекций области хирургического вмешательства в отдельных исследованиях остается неустановленной. Значимость ограничения рутинного использования периоперационной антибиотикопрофилактики продиктована также одной устойчивой неблагоприятной особенностью современной клинической медицины, которая заключается в неуклонном росте уровня устойчивости возбудителей госпитальных инфекций к антимикробным препаратам [16–17]. К сожалению, в рекомендациях Федерации анестезиологов и реаниматологов России при операциях у лиц с сопутствующим ожирением и профессионального сообщества SOBA (Society for Obesity and Bariatric Anesthesia) позиция по использованию периоперационной антибиотикопрофилактики не оговаривается [18–19].
Цель исследования — определение необходимости периоперационной антибиотикопрофилактики при видеоэндоскопических операциях в бариатрической хирургии.
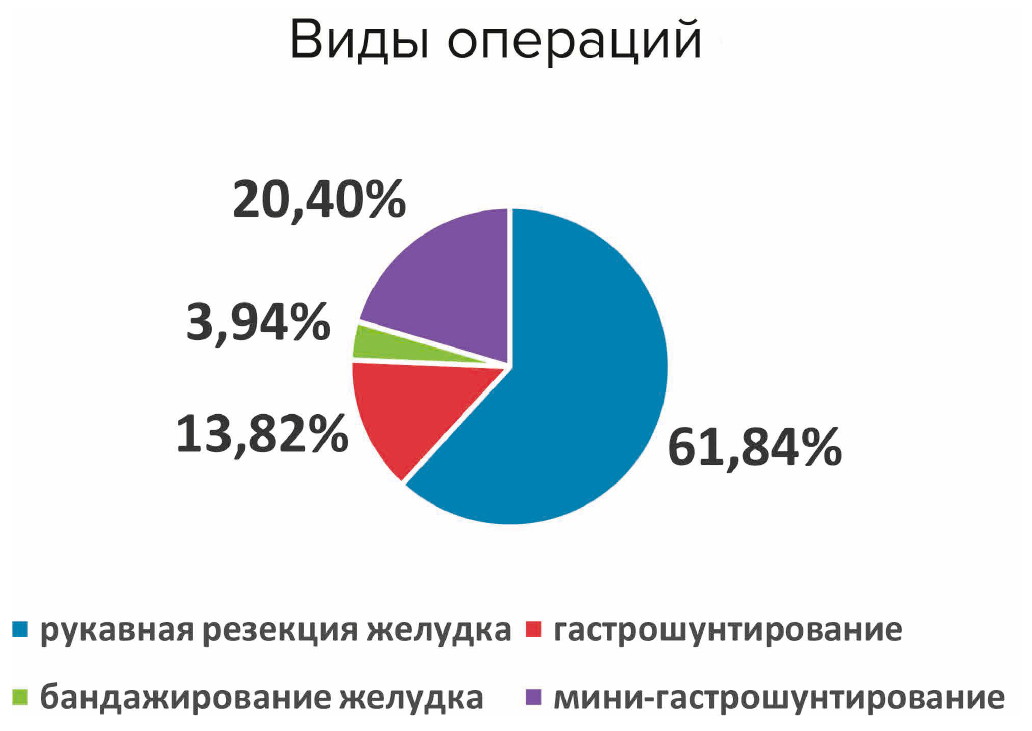
В обсервационное исследование включен 151 пациент, которому по поводу морбидного ожирения выполнены рукавная резекция желудка — 93 (61,84 %), гастрошунтирование — 21 (13,82 %), мини-гастрошунтирование — 31 (20,40 %) или бандажирование желудка — 6 (3,94 %) в условиях отсутствия периоперационной антибиотикопрофилактики (рис. 1).
Рис. 1. Виды оперативных вмешательств по поводу морбидного ожирения
Fig. 1. Types of surgical interventions for morbid obesity

Различные варианты консервативной терапии морбидного ожирения у данных лиц оказались неэффективны, и пациенты самостоятельно приняли решение о выполнении хирургического лечения. В предоперационном периоде проводилась оценка индекса массы тела, физического состояния по ASA (American Society of Anesthesiologists) и индексу коморбидности Charlson [20–21]. Наличие и тяжесть сопутствующих заболеваний устанавливались врачом-терапевтом соответствующего профиля и эндокринологом по существующим современным рекомендациям диагностики [22–23]. Среди сопутствующих заболеваний лидировали хроническая сердечная недостаточность — 53,94 % (82 человека) и сахарный диабет — 30,26 % (46 человек). Все оперативные вмешательства выполнялись одной бригадой хирургов. Для оценки риска инфекционных осложнений в области хирургического вмешательства использовали оригинальную шкалу BULCS и шкалу NNIS [24–25], а с целью диагностики инфекций области хирургического вмешательства — рекомендации Centers Disease Control, принятые и в России для оценки распространенности нозокомиальных инфекций [26]. Все операции выполнены под общей анестезией. Премедикация включала прием 0,02 мг/кг феназепама за 12 и 1 ч до операции. На операционном столе внутривенно пациенты получали 40 мг омепразола и 12 мг дексаметазона. Интраоперационный мониторинг включал в себя электрокардиографию, пульсовую оксиметрию, контроль частоты сердечных сокращений инвазивного или неинвазивного артериального давления. Индукция в анестезию проводилась фентанилом 5 мкг/кг и пропофолом 2 мг/кг. Интубация трахеи выполнялась под рокуронием 0,5–0,7 мг/кг, поддержание анестезии — севофлураном 1,5–2,0 объемных % и фентанилом — 15–20 мкг/кг. В ходе операции миоплегия поддерживалась рокуронием 0,15 мг/кг/ч. Параметры искусственной вентиляции легких: дыхательный объем — 500–650 мл; positive end expiratory pressure — 12–15 см вод. ст.; инспираторное давление — 30–35 см вод. ст., фракция кислорода во вдыхаемом воздухе составляла 50 %. Реверсия миоплегии выполнялась с помощью внутривенного введения сугаммадекса 150–200 мг.
Из 152 пациентов 150 экстубированы в операционном блоке спустя 20–40 мин после операции, двое из всей популяции оперированных больных в связи с запоздалым восстановлением адекватного спонтанного дыхания были транспортированы в палату реанимации. Исследование проводилось среди пациентов муниципального автономного учреждения городской клинической больницы № 40, подвергнутых хирургическому лечению по поводу избыточного веса или морбидного ожирения.
Критерии включения в исследование — все прооперированные пациенты, давшие согласие на оперативное лечение. В качестве материала для анализа были использованы медицинские карты. В разработку включались пациенты, оперированные в период с 8 августа 2016 г. по 10 ноября 2019 г. Из общего количества были исключены два пациента, так как в послеоперационном периоде им в течение 1–2 дней проводилось случайно назначенное профилактическое введение антибиотиков. В проводимом исследовании для статистической обработки полученных данных использовались программы Microsoft Excel 2013, EZRv.3.2.2 и MedCalcv.14.8.1 (Trialversion). С целью определения нормальности распределения данных использовался тест Шапиро—Уилка. Для оценки достоверности различий между качественными признаками использовался критерий хи-квадрат Пирсона (χ2) или точный критерий Фишера. Для всех статистических критериев ошибка первого рода устанавливалась равной 0,05. Непрерывные данные представлены M ± δ, где M — среднее арифметическое, δ — среднеквадратическое отклонение.
Средняя длительность перечисленных бариатрических операций составила 140,69 ± 35,57 мин. Подавляющее большинство пациентов относились к среднему возрасту — 44,0 ± 8,5 года (от 23 до 64 лет). Пациенты женского пола преобладали и составили 118 человек (78 %), мужчин было всего 34 человека (22 %). Средний индекс массы тела всех пациентов на момент поступления составил 46,56 ± 7,12 (95% ДИ; 33,5–71,8). По индексу коморбидности Charlson большинство пациентов относились к 1-му классу — 65 человек (43 %); ко 2-му классу — 30 человек (20 %). Пациентов, представляющих 3–4-й класс, было только 4 человека (3 %). Всего на долю лиц, не имеющих значимой сопутствующей патологии, приходилось 53 человека (35 %). Исходное физическое состояние по ASA у большинства пациентов относилось ко 2-му классу — 61 человек (40 %) и 3-му классу — 51 человек (34 %). Двадцать шесть человек (17 %) являлись предметом обсуждения нескольких специалистов и были отнесены консилиумом к 4-му классу по системе ASA. У них сохранялись проявления хронической сердечной недостаточности и выраженное снижение толерантности к физической нагрузке, что было связано с избыточной массой тела и рефрактерностью к проводимой терапии. Использование для предоперационной оценки функционального состояния 2 шкал прежде всего продиктовано наличием в системе коморбидности Charlson возраста и обширного круга нозологий, включающего инфаркт миокарда, хроническую обструктивную болезнь легких, сахарный диабет, цереброваскулярную болезнь, лейкемию и др.
Данная шкала позволяла расширить круг оценки, дав возможность полноценной характеристики исходного состояния. Однако с позиций риска инфекционных осложнений и потребности в пролонгированном введении антибиотиков в ближайшем послеоперационном периоде она не давала информации. В отличие от этой шкалы значения физического состояния ASA, указывающие на принадлежность к 4-му классу, могли служить основанием для назначения антибактериальных препаратов в периоперационном периоде, в особенности при наличии сочетания лейкоцитоза и субфебрильной температуры на третьи сутки с момента операции (рис. 2, 3).
Рис. 2. Уровень лейкоцитов крови после операции в зависимости от необходимости в эмпирической антибиотикотерапии
АБТ — антибиотикотерапия.
Fig. 2. The level of blood leukocytes after surgery, depending on the need for empiric antibiotic therapy
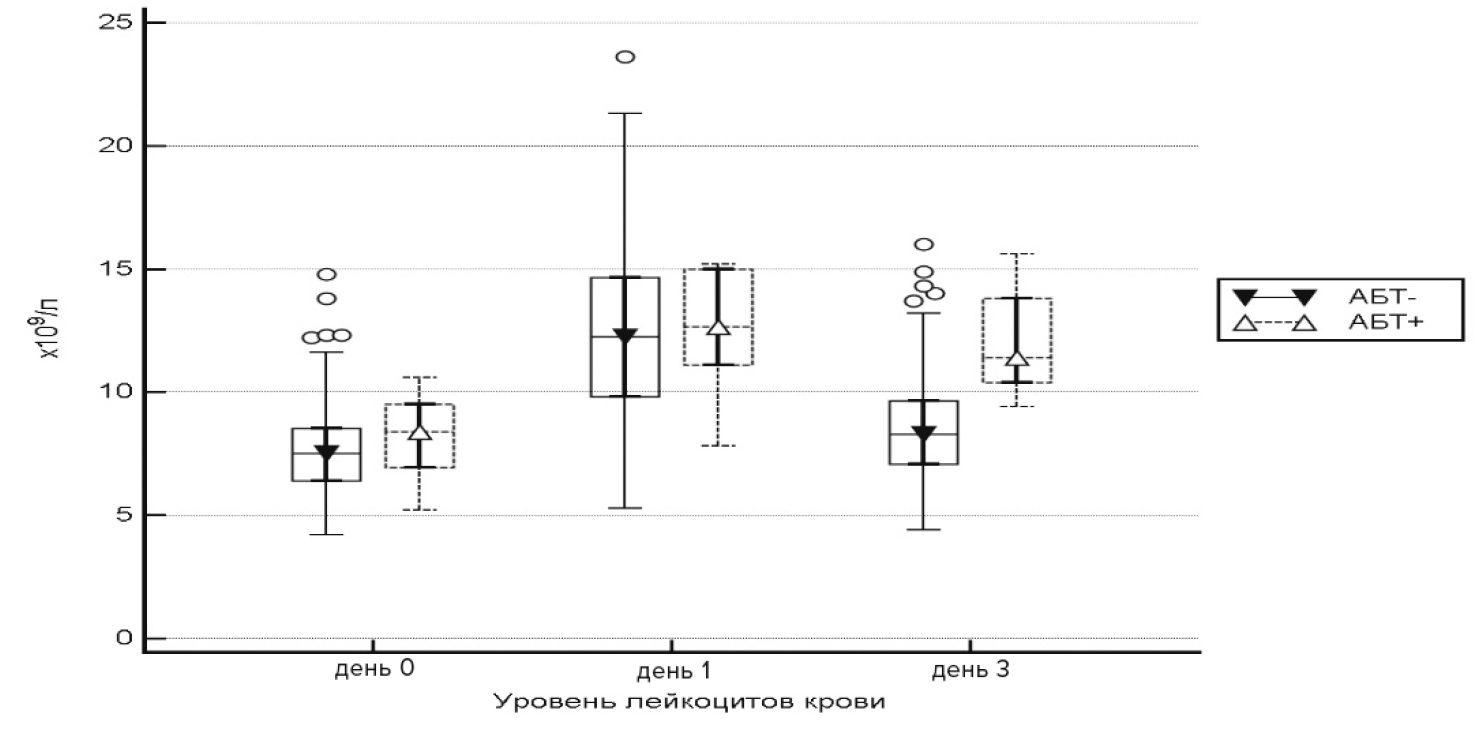
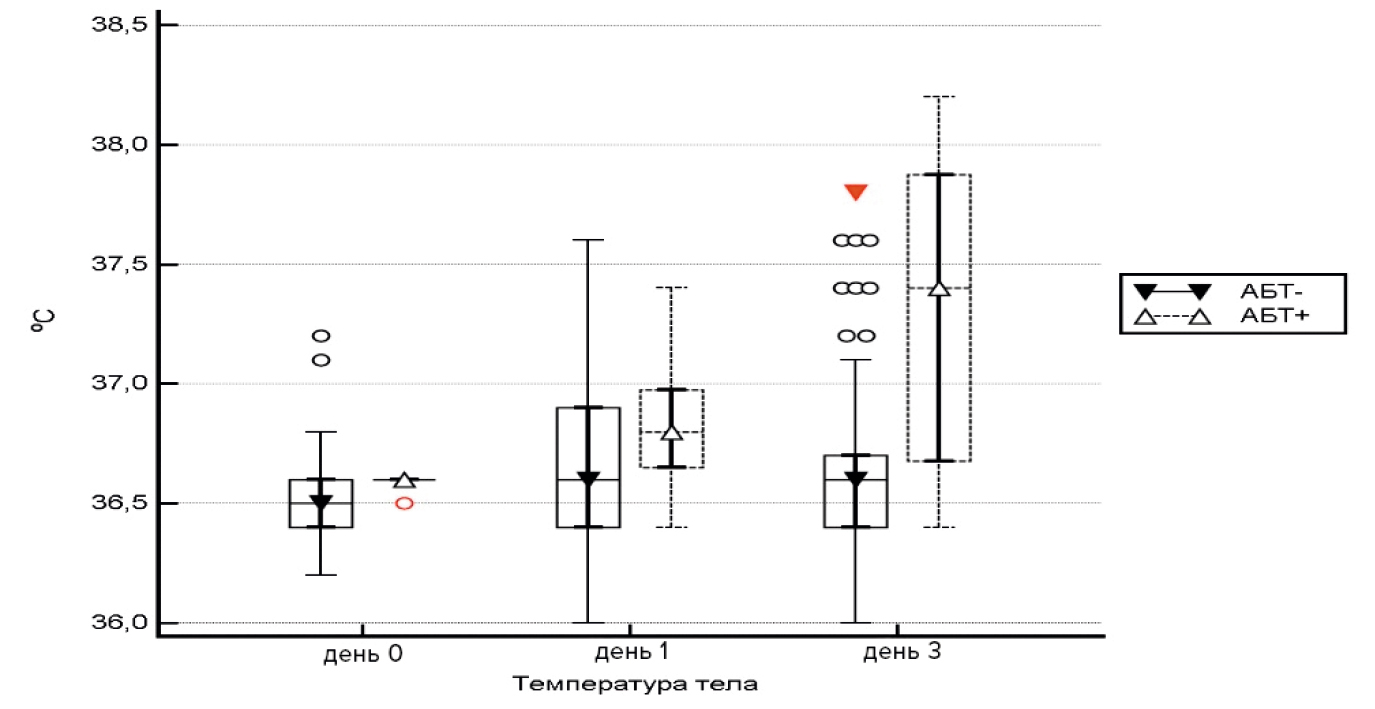
Рис. 3. Температура тела после операции в зависимости от необходимости в эмпирической антибиотикотерапии
АБТ — антибиотикотерапия.
Fig. 3. Body temperature after surgery, depending on the need for empirical antibiotic therapy
Отмеченная клинико-лабораторная симптоматика и вынужденная необходимость проведения эмпирического режима антибиотикотерапии в раннем послеоперационном периоде после эндовидеохирургических операций в бариатрии при отсутствии периоперационной профилактики возникли только у 7 пациентов (4,6 %). При этом отметим, что никакая из версий относительно локализации первичного очага не получила обоснования. Отсутствовали убедительные аргументы в пользу развития инфекции нижних дыхательных и мочевыводящих путей. Безусловно, можно предполагать существование транзиторной бактериемии, на что указывают Л.Л. Плоткин и соавт. после плановых операций в колопроктологии [27]. Между тем микробиологические доказательства ее развития в силу вскрытия кишечной трубки, выполненного хирургического вмешательства на желудке и кишечнике отсутствовали. В этих условиях нельзя полностью отрицать и формирование в результате операционной травмы в послеоперационном периоде системного воспаления неинфекционного генеза. Эмпирически назначался цефоперазон/сульбактам — 2 пациента; цефепим — 2 пациента и цефтриаксон — в 2 случаях внутривенно в максимальных дозах с учетом массы тела пациентов (цефепим — 6,0/сутки; цефтриаксон — 4,0/сутки). Длительность антибиотикотерапии препаратами класса β-лактамов, имеющими времязависимый киллинг, составляла 4–7 дней. У одного пациента наблюдалась несостоятельность анастомоза, что потребовало выполнения неотложной операции и соответствующего лечения. Согласно нашим данным, в качестве пороговой служит длительность операции более 180 мин (рис. 4). У одного пациента (0,66 %, 1/152) наблюдалась несостоятельность анастомоза, что требовало выполнения неотложной операции и соответствующего последующего лечения. Профилактическое назначение антибиотиков в данной клинической ситуации не играет определяющей роли. Согласно нашим данным, полученным в результате исследования, в качестве дополнительного фактора, указывающего на значимость лейкоцитоза и подъема температуры тела для назначения антибиотиков в послеоперационном периоде, служит и длительность операции более 180 мин (рис. 4).
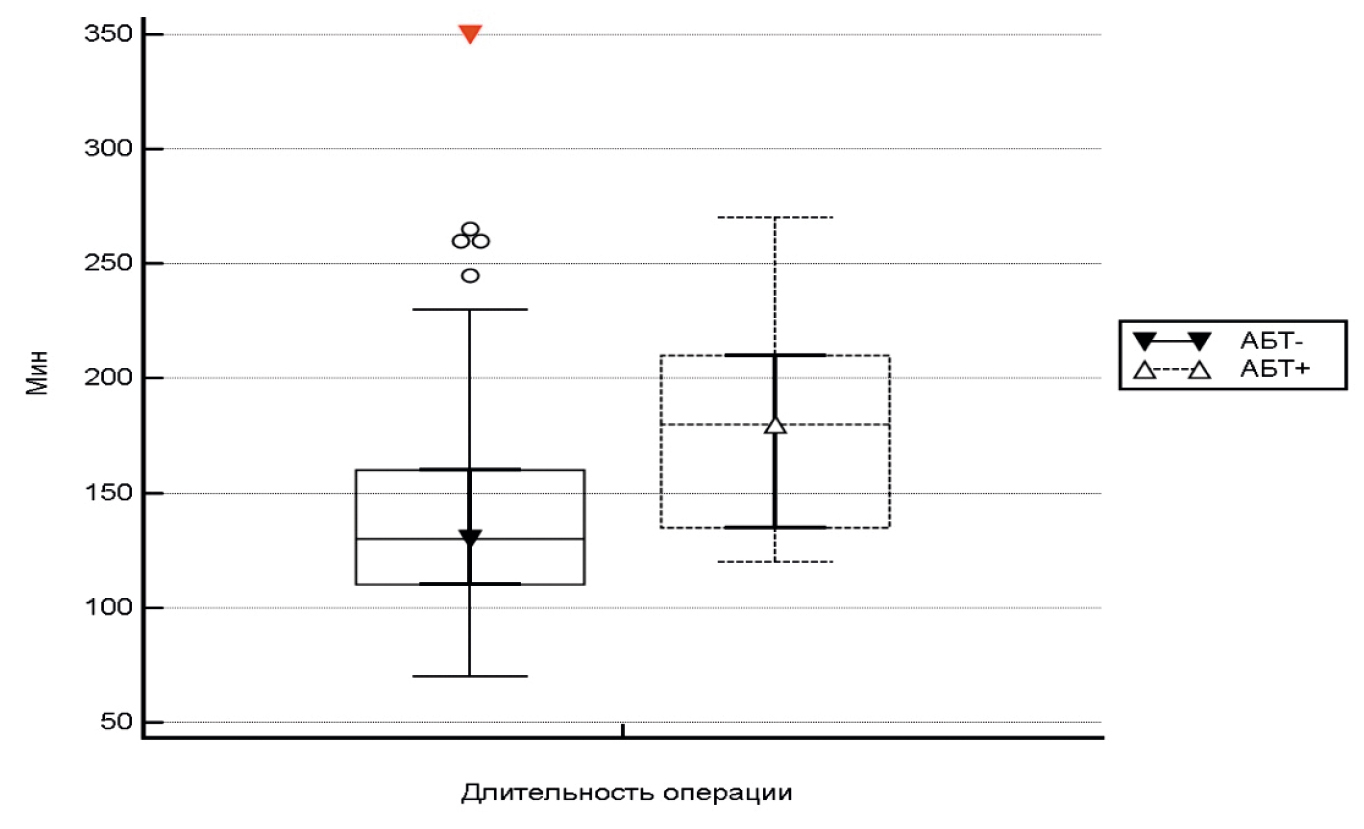
Рис. 4. Длительность операции (мин) и необходимость эмпирической антибиотикотерапии
АБТ — антибиотикотерапия.
Fig. 4. Duration of surgery (min) and the need for empiric antibiotic therapy
В целом проведение эмпирической антибиотикотерапии сопровождается увеличением необходимости госпитализации в стационар в среднем на 7 дней (р < 0,001) и, по-видимому, повышает материальные затраты стационара. Можно предположить, что в периоперационной антибиотикопрофилактике нуждаются пациенты при их отнесении в исходном состоянии к 4‑му классу по ASA и превышении длительности операции в 3 ч. Между тем продолжительность оперативного вмешательства не всегда возможно предсказать.
По результатам нашего исследования мы полагаем, что при использовании эндовидеохирургической техники в бариатрии периоперационная антибиотикопрофилактика не является обязательной для всей популяции лиц, подвергнутых хирургическому лечению. Идеальным было бы проведение полноценного многоцентрового сравнительного исследования. Однако, принимая во внимание отсутствие инфекции области хирургического вмешательства и низкую частоту синдрома системного воспаления в раннем послеоперационном периоде, его реализация крайне сомнительна. Ориентация в послеоперационном периоде на конкретные цифровые значения температуры тела, лейкоцитоза при наличии факторов риска больше служит основанием для наблюдения и дополнительного обследования и отдается на выбор врача в отношении старта эмпирической антибиотикотерапии.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов. Прудков А.И., Анферов И.Д., Анферов Д.И., Федорова К.Е., Мезенина Я.М., Струихин А.С., Нишневич Е.В., Руднов В.А. — разработка концепции статьи, получение и анализ фактических данных, написание и редактирование текста статьи, проверка и утверждение текста статьи.