Высокая вероятность развития при сепсисе нарушения функции миокарда, т. е. септической кардиопатии (СКП), в настоящее время не вызывает сомнений [1–5]. Вместе с тем функционально-диагностические признаки, позволяющие выявлять ранние стадии СКП, остаются предметом дискуссии [6, 7]. Одним из направлений в изучении этой проблемы является прикроватная эхокардиография (ЭхоКГ) [8]. Опубликованы сообщения о высокой информативности в диагностике СКП современных показателей ЭхоКГ, характеризующих систолическую и диастолическую функцию левого желудочка (ЛЖ), систолическую функцию правого желудочка, изменения желудочково-артериальной связи и др. [6]. Однако их реализация в условиях отделения реанимации и интенсивной терапии (ОРИТ) требует привлечения высококвалифицированных специалистов и использования аппаратуры экспертного класса [9].
В российских ОРИТ общего профиля прикроватная ЭхоКГ не является рутинной диагностической процедурой, ее выполнение нередко сталкивается с административно-организационными и кадровыми трудностями. Специалист, выполняющий ЭхоКГ в ОРИТ, в большинстве случаев регистрирует более или менее ограниченный спектр показателей. Наряду с визуальным изучением функции клапанов, сегментарной сократимости стенок ЛЖ и наличия выпота в полости перикарда, определяют заполнение ЛЖ, путем измерения его конечно-диастолического и конечно-систолического объемов (КДОЛЖ и КСОЛЖ), а систолическую функцию ЛЖ оценивают по его фракции изгнания (ФИЛЖ) [10].
Дилатацию ЛЖ и снижение ФИЛЖ традиционно считают признаками СКП [3, 4, 11], однако прогностическая значимость этих изменений в отношении риска летальности остается неясной. Одни авторы подчеркивают, что вновь возникшее при сепсисе уменьшение ФИЛЖ повышает риск летальности [12], другие указывают на низкую предикторную ценность этого признака [13]. Некоторые эксперты пытаются трактовать дилатацию ЛЖ со снижением ФИЛЖ до уровня менее 45 % как благоприятную адаптационную реакцию сердца, снижающую риск летальности [2]. Такая интерпретация данных ЭхоКГ затрудняет адекватную оценку клинической ситуации и выбор оптимальной лечебной тактики.
Тем не менее прикроватную ЭхоКГ в последние годы нередко позиционируют как альтернативу измерению центрального венозного давления и инвазивному мониторингу центральной гемодинамики (ЦГД) в целом [8]. Такой вариант последнего, как транспульмональная термодилюция (ТПТД), вполне приемлем для использования в ОРИТ общего профиля и позволяет получить объективную информацию о насосной функции сердца, в том числе при сепсисе [14]. Показано, что результаты оценки состояния больного в ОРИТ с помощью ТПТД и ЭхоКГ могут в отдельных наблюдениях не совпадать [15], однако вопрос о том, какой метод обладает большей диагностической ценностью, остается открытым [16], особенно если используется ограниченный протокол ЭхоКГ.
Изложенное определило цель исследования — изучить соответствие друг другу показателей, регистрируемых с помощью прикроватной ЭхоКГ и ТПТД у больных с абдоминальным сепсисом, и оценить их предикторную значимость в отношении риска летальности.
В соответствии с разрешением этического комитета ФУВ ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, протокол № 11 от 13.12.2018, выполнили одноцентровое простое проспективное обсервационное исследование. Критерии включения в последнее: абдоминальный сепсис, возраст 18–85 лет, наличие письменного информированного согласия больных на использование мер интенсивного наблюдения, обследования и лечения, включая инвазивный мониторинг ЦГД с помощью ТПТД. Критерии невключения: анамнестические данные о наличии у больного хронической недостаточности кровообращения, беременность, терминальная стадия онкологических заболеваний, тяжелые заболевания эндокринной системы, черепно-мозговая или сочетанная травма, терминальная стадия хронических легочных заболеваний. Критерии исключения: пороки клапанного аппарата сердца, фибрилляция предсердий, нарушения сегментарной сократимости стенок ЛЖ, противопоказания к катетеризации бедренной артерии или невозможность выполнить эту процедуру.
Обследовали 25 больных (15 мужчин и 10 женщин) в возрасте 20–83 (45 [31; 68]) лет с абдоминальным сепсисом или септическим шоком, диагностированными в соответствии с критериями «Сепсис-3» [17]. У больных диагностировали: острый деструктивный панкреатит (n = 10), острый аппендицит (n = 5), перфоративную язву желудка или двенадцатиперстной кишки (n = 3), перфорацию кишечника (n = 1), острый холецистит и/или холангит (n = 6). Тяжесть состояния при поступлении в ОРИТ по шкале APACHE II составила 6–20 (13 [11–16]; 13,3 ± 0,7) баллов, по шкале SOFA — 2–12 (8 [6,5–9,5]; 8,0 ± 2,6) баллов. Симпатомиметические препараты были назначены в 17 (68 %) наблюдениях; гиперлактатемию в пределах 2,2–5,2 (2,9 [2,8–3,7]; 3,2 ± 0,9) ммоль/л выявили у 14 (56 %) больных. По совокупности клинико-лабораторных показателей в соответствии с критериями «Сепсис-3» [17] у 13 (52 %) больных диагностировали септический шок. Летальность в ОРИТ составила 28 % (7 больных).
Больные получали стандартное интенсивное лечение, включавшее инфузию сбалансированных кристаллоидных растворов, стартовую деэскалационную антибиотикотерапию с дальнейшей сменой препаратов согласно результатам бактериологических посевов биологических сред и другие лечебные меры. Инфузии и назначение симпатомиметических препаратов выполняли в соответствии с протоколом коррекции нарушений в системе кровообращения по рекомендациям «Сепсис-3» [17].
В анализ включили данные ЭхоКГ и ТПТД, зарегистрированные одновременно в первые 24 ч нахождения больных в ОРИТ. Прикроватную ЭхоКГ выполняли с помощью портативного ультразвукового аппарата Vivid I (GE Healthcare), располагая датчик в трех стандартных позициях (парастернальная, апикальная, субкостальная). КДОЛЖ, КСОЛЖ и ФИЛЖ определяли в В-режиме по методу Симпсона (метод «дисков»). Ударный объем (УО) ЛЖ определяли по уравнению непрерывности потока (УО = интеграл линейной скорости потока в выносящем тракте ЛЖ × площадь поперечного сечения выносящего тракта ЛЖ). Сердечный выброс рассчитывали по формуле: УО × частота сердечных сокращений (ЧСС). Оценивали локальную сократимость миокарда ЛЖ, толщину стенок ЛЖ и состояние клапанного аппарата сердца. В анализ включили: индексы КДОЛЖ (ИКДОЛЖ), КСОЛЖ (ИКСОЛЖ) и УО (ИУОэхо), ФИЛЖ и сердечный индекс (СИэхо). Нормальными считали ИКДОЛЖ 35–75 мл/м, ИКСОЛЖ 12–30 мл/м2 и ФИЛЖ > 55 % [18].
Всем больным выполняли катетеризацию магистральной вены (подключичная и/или внутренняя яремная) и бедренной артерии катетером Pulsiocath PV2015L204F (Pulsiоn Medical Systems), который соединяли с модулем PiCCO-plus (Pulsiоn Medical Systems) мониторной системы фирмы Drager. ТПТД осуществляли по стандартной методике [14]. Регистрировали: ЧСС, СИ (СИтптд), ИУО (ИУОтптд), индекс глобального конечно-диастолического объема (ИГКДО), глобальную фракцию изгнания сердца (ГФИС), индекс функции сердца (ИФС) и индекс общего периферического сосудистого сопротивления. Рассчитывали инотропный индекс (ИИ) и вазоактивно-инотропный индекс (ВИИ) [19] по формулам:
Для хранения и обработки данных использовали базу данных, сформированную в программе Microsoft Office Excel. Статистический анализ выполнили с помощью программных пакетов Microsoft Office Excel и MedCalc 15.
Учитывая ограниченный объем выборки, характер распределения данных анализировали с помощью критериев Шапиро—Уилка, Шапиро—Франка и Д’Агостино—Пирсона. Все данные представили в виде медианы (Me) и интерквартильного интервала (P25–P75). Данные, имевшие нормальное распределение, дополнительно представили в виде среднеарифметических величин (M) и среднеквадратичных отклонений (σ). Рассчитывали среднюю частоту признаков (Р). Отличия данных несвязанных выборок оценивали по критерию Манна—Уитни, отличия частотных признаков — с помощью точного критерия Фишера. Отличия считали значимыми при вероятности ошибки менее 5 % (р < 0,05).
Рассчитывали коэффициенты ранговой корреляции Спирмена (rho). Если оба коррелируемых показателя имели нормальное распределение, дополнительно рассчитывали коэффициент корреляции Пирсона (r). Оценивали 95%-й доверительный интервал (ДИ) и величину р. При значениях rho (r) < 0,3 связь считали слабой, при значениях 0,3–0,7 — умеренной, более 0,7 — сильной.
С помощью логистической регрессии оценивали влияние независимых переменных на зависимую (исход заболевания или другой изучаемый признак), закодированную в бинарном виде. Рассчитывали отношение шансов (ОШ), 95% ДИ и значимость влияния (р). Для оценки разделительной способности независимых переменных выполнили ROC-анализ, в который включали показатели, влиявшие на зависимую переменную. Анализировали характеристики ROC-кривых с расчетом площади под кривой (ППК), 95% ДИ и статистической достоверности (p) выявленной зависимости. Качество модели считали при ППК > 0,9 — отличным, 0,8–0,9 — очень хорошим, 0,7–0,8 — хорошим, 0,6–0,7 — средним, 0,5–0,6 — неудовлетворительным. Пороговое значение (ПЗ) переменной (порог отсечения, точка cut-off) определяли по индексу Юдена (требование максимальной суммы чувствительности и специфичности), требованию чувствительности теста, приближающейся к 80 %, и требованию баланса между чувствительностью и специфичностью (минимальная разность между этими значениями). За ПЗ принимали значение, в наибольшей степени соответствующее всем трем требованиям.
На фоне умеренной тахикардии медианы и средние величины показателей прикроватной ЭхоКГ и ТПТД соответствовали диапазону нормальных значений, установленных для обоих методов (табл. 1). Значения ИИ соответствовали умеренной инотропной поддержке, а ВИИ указывал на значительные дозы вазопрессорных симпатомиметических препаратов, использовавшихся в момент исследования.
Все выявленные корреляционные связи (табл. 2) были умеренными. Коррелировали значения СИ и ИУО, установленные с помощью ЭхоКГ и ТПТД. Отметили корреляции между объемами ЛЖ и ИГКДО, а также между ФИЛЖ и ГФИС. С ИИ обратно коррелировали СИтптд и ИФС. С ВИИ не коррелировал ни один из изученных параметров, хотя и прослеживалась тенденция (р < 0,1) к корреляции ИИ и ВИИ с СИэхо.
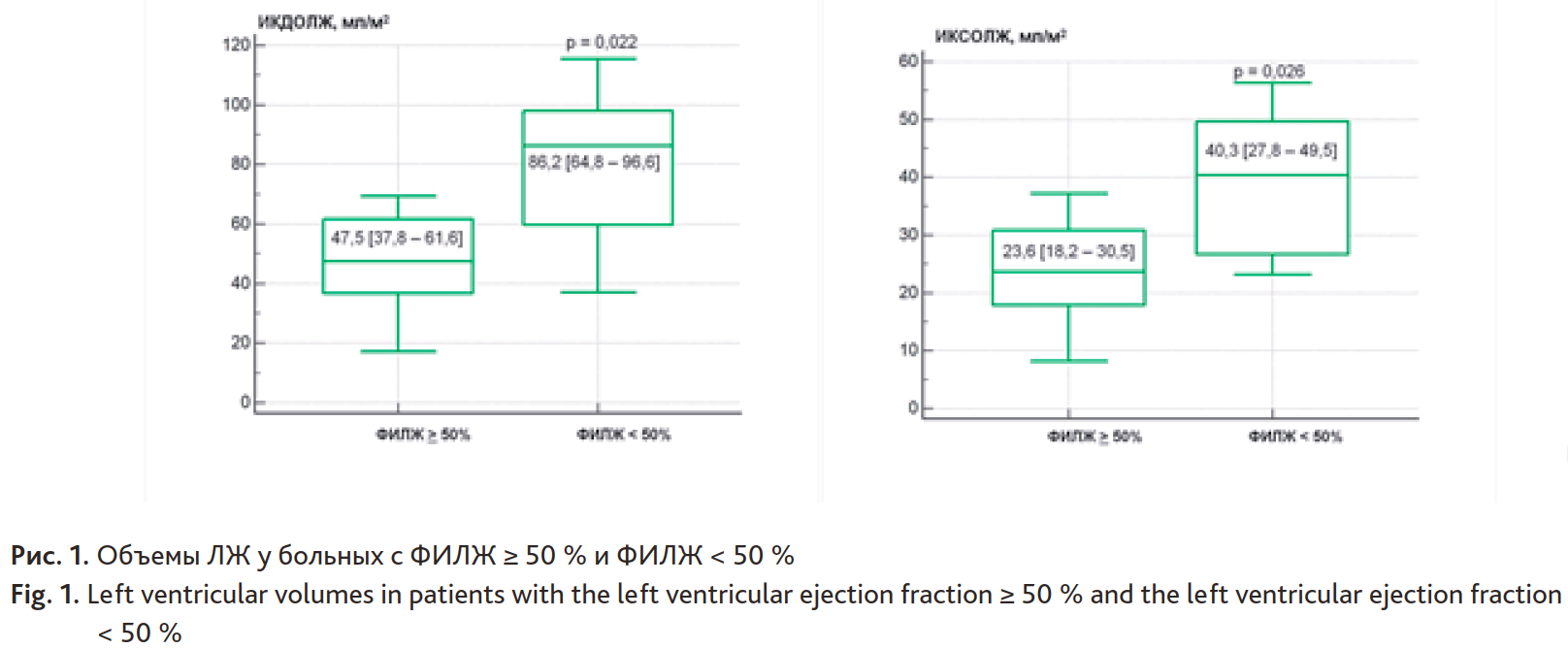
Дилатацию ЛЖ (ИКДОЛЖ 80–115 мл/м2) выявили у 4 (16 %) больных. Повышенный уровень ИКСОЛЖ (32–56 мл/м2) зарегистрировали в 9 (36 %) наблюдениях. Снижение ФИЛЖ до уровня менее 50 % (48–23 %) выявили в 6 (24 %) наблюдениях. У больных со сниженной ФИЛЖ, по сравнению с остальными, были увеличены ИКДОЛЖ и ИКСОЛЖ (рис. 1). Вместе с тем уменьшение ФИЛЖ сочеталось с дилатацией ЛЖ (ИКДОЛЖ > 75 мл/м2) только в 4 (16 %) наблюдениях.
Сниженные значения CИэхо (< 2,5 л/мин/м2) зарегистрировали у 7 (28 %) больных. СИэхо умеренно коррелировал с ФИЛЖ (рис. 2): rho 0,410; 95% ДИ 0,018–0,693; р = 0,042. Вместе с тем ФИЛЖ не была ассоциирована со снижением СИэхо: ОШ 0,9323; 95% ДИ 0,8574–1,0136; р = 0,10. Между СИэхо и объемами ЛЖ корреляции не было (rho 0,235 и 0,338; р> 0,05). При выполнении ТПД сниженный СИ (CИтптд < 2,5 л/мин/м2) выявили в 8 (32 %) наблюдениях. ФИЛЖ не ассоциировалась с CИтптд < 2,5 л/мин/м2: ОШ 0,9807; 95% ДИ 0,9090–1,0580; р = 0,6141. Ни один из показателей ТПТД не был ассоциирован c ФИЛЖ < 50 % (табл. 3).
Предиктором летального исхода (табл. 4) был только ИФС. Ни один из остальных показателей, включая фармакологические индексы, не был ассоциирован с летальностью. У больных с ФИЛЖ < 50 % летальность составила 33 %, а в наблюдениях с ФИЛЖ > 50 % — 26,3 % (p = 0,851). Также констатировали, что у больных с дилатацией ЛЖ (ИКДОЛЖ > 75 мл/м2) летальность составила 50 %, а в наблюдениях, где ИКДОЛЖ был нормальным, — 24 % (р = 0,548).
При ROC-анализе разделительной способности ИФС в отношении летальности ППК составила 0,817 (95% ДИ 0,613–0,942; р = 0,0057), что соответствовало модели очень хорошего качества (рис. 3). ПЗ ИФС < 5,8 мин–1 с чувствительностью 85,7 % и специфичностью 72,2 % являлось предиктором летального исхода. Среди больных с ИФС < 5,8 мин–1 летальность составила 71 %, среди остальных — 5,9 % (р = 0,002).
Прежде всего отметим, что в последние годы ЭхоКГ и ТПТД стали нередко противопоставлять друг другу [15, 16], особенно в рамках активно рекомендуемой «экскалационной тактики» мониторинга при сепсисе. В процессе реализации такой тактики должен происходить переход от «простых к сложным» мониторным методикам: от общеклинической оценки состояния больного к прикроватной ЭхоКГ, а затем, только при ухудшении состояния и прогрессировании нарушений кровообращения, — к инвазивному мониторингу ЦГД в варианте ТПТД [8, 16]. При этом вопрос о диагностической ценности для выявления СКП стандартных показателей ЭхоКГ и ТПТД, доступных в рутинной клинической практике ОРИТ общего профиля, и их предикторная ценность в отношении летальности остается открытым. Поэтому в рамках выполненной работы анализировали не только корреляции между регистрируемыми параметрами, но и их способность выделить больных с высоким риском неблагоприятного исхода сепсиса.
Сведения о корреляции между величинами СИ и/или ИУО, определенными при ЭхоКГ и с помощью термодилюции, крайне немногочисленны. Например, у больных дилатационной кардиомиопатией при использовании препульмональной термодилюции (катетер Свана—Ганза) показатели не коррелировали [20]. Авторы допускали, что для этого могли быть технические причины. При целенаправленной сравнительной оценке значений СИ, измеренного с помощью препульмональной термодилюции и ультразвуковой допплерографии во время кардиохирургических операций, авторы продемонстрировали умеренную корреляцию величин [21]. Выявленные в настоящем исследовании корреляционные связи указывали на умеренное соответствие результатов оценки ЦГД с помощью ЭхоКГ и ТПТД. Корреляции не только в парах ИУОэхо–ИУОтптд и СИэхо–СИтптд, но и между показателями, имеющими сходный физиологический смысл (ФИЛЖ–ГФИС, ИГКДО–ИКДОЛЖ и ИГКДО–ИКСОЛЖ), подтверждают, что индексы, вычисляемые при ТПТД путем математических экстраполяций по специальным формулам [14], достаточно адекватно характеризуют ЦГД при сепсисе.
Корреляции между ИГКДО и объемами ЛЖ ранее практически не изучались, но можно полагать, что наличие этих связей вполне закономерно, учитывая, что все показатели характеризуют заполнение камер сердца кровью. Корреляция между ГФИС и ФИЛЖ описана: при сепсисе эта связь тесная [22], а при кардиогенном шоке — умеренная [23], что соответствует данным настоящего исследования.
Умеренная выраженность всех корреляций не только указывает на наличие определенных взаимосвязей между изучаемыми показателями, но и свидетельствует о самостоятельной диагностической ценности каждого из методов. Например, полученные данные не дают оснований уверенно рекомендовать замену термодилюционного определения СИ ультразвуковой оценкой УО с помощью прикроватной ЭхоКГ.
Отдельного обсуждения заслуживает ИФС, который у обследованных больных не коррелировал ни с одним из параметров ЭхоКГ. Немногочисленные авторы, сравнившие ИФС с ФИЛЖ, констатировали наличие корреляции между показателями. Вместе с тем было показано, что у больных с сепсисом корреляция между ФИЛЖ и ИФС выражена значительно слабее, чем между ФИЛЖ и ГФИС [22]. У ИФС нет прямых аналогов, регистрируемых при ЭхоКГ. Принимая во внимание формулу расчета ИФС (СИ/ИГКДО), куда входит характеристика глобальной преднагрузки (ИГКДО) [14], отметим, что параметр в наибольшей степени близок к насосным коэффициентам желудочков [24]. Эти показатели призваны оценивать ударную работу сердца при определенном уровне преднагрузки во время каждого сокращения. Можно полагать, ИФС при сепсисе отражает не только систолическую функцию миокарда, как принято считать [22, 23, 25], но и эффективность реализации преднагрузки, зависящей в том числе от динамики миокардиального расслабления. Нарушение последнего (диастолическая дисфункция) является типичным признаком СКП [3, 5, 6]. Таким образом, в отличие от ГФИС и ФИЛЖ, ИФС характеризует и систолическую, и диастолическую функцию миокарда. Аналогичной диагностической ценностью обладает, например, индекс производительности миокарда ЛЖ («индекс Tei»), рассчитываемый из соотношения времени изоволюмического сокращения, времени изгнания и времени изоволюмического расслабления, определенных при ультразвуковой допплерографии. Этот индекс, выявляющий и систолическую гипофункцию ЛЖ, и диастолическую дисфункцию, обладает высокой информативностью для выявления СКП [26].
Установленная частота уменьшения ФИЛЖ (24 %) совпала с суммарной частотой различных вариантов систолической дисфункции ЛЖ, отмеченной в одном из исследований, посвященных выявлению СКП [5]. Следует отметить, что выявляемость сниженной ФИЛЖ при сепсисе варьируется в широких пределах: от 15 до 48 % [11, 27]. Как правило, снижение ФИЛЖ как признак СКП связывают с дилатацией ЛЖ [2–4, 11]. По данным настоящего исследования, объемы ЛЖ у больных с ФИЛЖ < 50 % были заметно выше, чем у остальных. Вместе с тем уменьшение ФИЛЖ сочеталось с патологическими значениями ИКДОЛЖ (> 75 мл/м2) в небольшом числе наблюдений.
Выраженное увеличение ИКДОЛЖ (около 159 мл/м2) у большинства (59 %) обследованных больных с сепсисом было выявлено в единственном исследовании, выполненном с помощью радионуклидной вентрикулографии [11]. В настоящее время такую дилатацию ЛЖ при СКП практически не описывают. Например, с помощью ЭхоКГ умеренную степень дилатации ЛЖ регистрируют в 11 % наблюдений [28], что практически соответствует нашим данным. В ряде исследований, авторы которых зарегистрировали снижение ФИЛЖ при сепсисе, выраженная дилатация ЛЖ также не описана. Средние значения ИКДОЛЖ находятся либо в пределах, либо на верхней границе физиологической нормы: 61 ± 17 — 76 ± 18 мл/м2 [29–32]. Можно констатировать, что описание дилатации ЛЖ как признака СКП в большинстве исследований базируется на отличиях ИКДОЛЖ между группами больных, выделенных по признаку разной ФИЛЖ, летальности и др. При этом больший ИКДОЛЖ в одной из групп трактуется как дилатация ЛЖ, даже если этот объем находится в пределах физиологической нормы. С практической точки зрения важно, что регистрация у больного с сепсисом формально нормальных уровней ФИЛЖ и/или ИКДОЛЖ не исключает наличия СКП.
У обследованных нами больных нередко выявляли патологический уровень ИКСОЛЖ (> 30 мл/м2). Вместе с тем частота повышенного ИКСОЛЖ не отличалась от выявляемости патологических значений ИКДОЛЖ (р = 0,213), что, возможно, было обусловлено ограниченным числом наблюдений. Характеризуя объемы ЛЖ при СКП, исследователи крайне редко указывают значения ИКСОЛЖ, хотя его повышение является не менее важной, чем увеличенный ИКДОЛЖ, характеристикой дисфункции сердца и важным фактором уменьшения ФИЛЖ. В одном из исследований [29] у больных с ИКДОЛЖ около 75 мл/м2 средний ИКСОЛЖ превышал 40 мл/м2, что являлось несомненной причиной снижения ФИЛЖ. Еще в одном исследовании у больных с СКП была не только снижена ФИЛЖ, но и увеличен конечно-систолический размер ЛЖ [33]. Можно полагать, что при верификации СКП следует большее внимание уделять значениям ИКСОЛЖ. Показано, что при оценке степени нарушения ЦГД у больных сердечной недостаточностью ИКСОЛЖ в два раза чувствительнее, чем ФИЛЖ [20].
При дилатационной кардиомиопатии продемонстрирована достаточно выраженная корреляция между ФИЛЖ и СИэхо [20]. В нашем исследовании связь ФИЛЖ с СИэхо была умеренной, причем ФИЛЖ не была ассоциирована с уровнем СИэхо < 2,5 л/мин/м2. Вполне вероятно, что при сепсисе в условиях резких изменений постнагрузки и преднагрузки [1], сила прямой связи между показателями систолической функции и общей производительности сердца уменьшается. Также мы не отметили ассоциированности параметров ТПТД со сниженной ФИЛЖ (< 50 %), на что указывают отдельные авторы [22]. Нельзя исключить, что такая ассоциированность могла бы проявиться при использовании в качестве зависимой переменной уровня ФИЛЖ < 40 или < 30 %, однако среди обследованных больных такая степень уменьшения ФИЛЖ была крайне редкой.
Исследования, посвященные сравнительной информативности прикроватной ЭхоКГ и ТПТД при интенсивной терапии больных с сепсисом, крайне немногочисленны. В одном из них на основании данных указанных методов эксперты делали заключение о состоянии больного и целесообразных лечебных мерах [15]. В результате установили, что непосредственно в ОРИТ частота совпадения экспертных заключений была лишь удовлетворительной и возрастала при повторном отсроченном анализе. Корректность интерпретации данных специальных методов обследования не влияла на уровень лактатемии и летальность. Анализируя это исследование, следует отметить, что, оценивая состояние кровообращения, эксперты стремились достичь уровня показателей, характерного для физиологической нормы [15]. Целесообразность обеспечения у больных с сепсисом нормального физиологического уровня показателей ЦГД вызывает определенные сомнения. Для сепсиса характерна определенная «стресс-норма» показателей ЦГД, когда значения, предсказывающие неблагоприятный исход, нередко находятся в середине диапазона нормальных значений [34].
Установление параметров, указывающих на риск неблагоприятного исхода сепсиса, необходимо для повышения эффективности цель-ориентированной коррекции ЦГД. Ни один из показателей, зарегистрированных на раннем этапе интенсивной терапии сепсиса с помощью прикроватной ЭхоКГ, включая ФИЛЖ, не был ассоциирован с летальностью. С другой стороны, сниженная ФИЛЖ не была и признаком, предсказывающим благоприятный исход сепсиса, как иногда указывают [2]. Предикторная значимость ФИЛЖ у больных с сепсисом остается предметом дискуссии. Опубликованы данные, что вновь возникшее снижение ФИЛЖ значимо повышает риск летальности [12]. Вместе с тем современный метаанализ продемонстрировал крайне низкую чувствительность и специфичность ФИЛЖ как предиктора неблагоприятного исхода [13]. Наиболее вероятно, что умеренное снижение ФИЛЖ не обладает достаточной информативностью как признак выраженности СКП. Вместе с тем нельзя исключить, что резко выраженное снижение или, напротив, супранормальное повышение ФИЛЖ [11] может указывать на неблагоприятный прогноз.
Единственным предиктором летального исхода у обследованных больных был уровень ИФС < 5,8 мин–1. Это значение, находящееся в середине диапазона нормальных значений (4,5–6,5 мин–1) [14]. Ряд авторов указывал на информативность ИФС для выявления СКП [22, 25]. Есть основания полагать, что определенный уровень ИФС, выявляемый на ранних стадиях сепсиса, может стать ориентиром для целенаправленной коррекции ЦГД. Нуждаются в целенаправленном изучении и другие показатели. С помощью ТПТД на самых ранних стадиях интенсивного лечения абдоминального сепсиса можно выявить ряд параметров, ассоциированных с летальностью [34].
В связи с этим реализация «экскалационной тактики» мониторинга при сепсисе [8, 16] в отечественных ОРИТ вызывает определенные возражения. Не обсуждая организационно-кадровые вопросы, отметим, что даже своевременно выполненная прикроватная ЭхоКГ не всегда способна адекватно оценить состояние больного, так как стандартно определяемые показатели могут не обеспечить корректной оценки выраженности СКП и не помочь в прогнозировании рисков. Кроме того, диагностическая ценность и объем получаемой при ЭхоКГ информации зависят от качества аппаратуры, наличия ультразвукового окна у конкретного больного и квалификации исследователя. В результате корректность оценки состояния ЦГД и, главное, оперативное начало или изменение необходимых лечебных мер становятся проблематичными. Полагаем, что более перспективным в такой клинической ситуации может оказаться «опережающая» тактика, направленная на выявление с помощью ТПТД ранних проявлений СКП и их коррекцию. Безусловно, инвазивный мониторинг ЦГД не показан всем больным с сепсисом, но и его начало только у крайне тяжелых больных с септическим шоком и рефрактерностью к симпатомиметикам вряд ли оправданно. Необходимо установление объективных показаний к началу развернутого мониторинга, когда показатели кровообращения еще вполне удовлетворительны, но прогрессирование СКП и неблагоприятный прогноз становятся высоковероятными, т. е. поиск «негемодинамических» предикторов СКП. Такими предикторами могут быть, например, различные лабораторные маркеры и др. Данные настоящего исследования не дают оснований рекомендовать ультразвуковую оценку объемов заполнения ЛЖ и ФИЛЖ в качестве неинвазивной альтернативы ТПТД. Вместе с тем прикроватная ЭхоКГ с использованием аппаратуры экспертного класса и современных диагностических методик, способных выявить ранние ультразвуковые признаки СКП [6, 26], несомненно, заслуживает внедрения в практику отечественных ОРИТ общего профиля.
Завершая обсуждение, отметим, что в настоящем исследовании не стояла цель выполнить тщательную оценку соответствия измерений, получаемых с помощью различных методов мониторинга. Оба метода имеют заслуженную высокую репутацию и, несомненно, способны предоставить содержательную информацию о функции сердца. Вместе с тем ряд параметров, регистрируемых с помощью и ЭхоКГ, и ТПТД не обладает предикторной способностью в отношении неблагоприятного исхода сепсиса. Мы далеки от мысли противопоставлять ЭхоКГ и ТПТД и считаем, что наиболее конструктивный подход заключается в выявлении показателей, указывающих на риск летальности.
Полагаем, что у настоящего исследования имеются следующие ограничения: ограниченная выборка клинических наблюдений, невозможность выполнить и проанализировать данные ЭхоКГ экспертного уровня, выполненной с использованием специальных углубленных методик оценки систолической и диастолической функции миокарда желудочков.
Суммируя результаты настоящего исследования, можно заключить, что у обследованных больных с сепсисом показатели насосной функции сердца (СИ и ИУО), а также параметры, имеющие сходный физиологический смысл (ФИЛЖ и ГФИС, ИГКДО, ИКДОЛЖ и ИКСОЛЖ), определенные одновременно с помощью прикроватной ЭхоКГ и ТПТД в первые 24 ч нахождения больных в ОРИТ, коррелировали между собой. Частота снижения ФИЛЖ до уровня < 50 % составила 24 %, однако ни ФИЛЖ, ни объемы заполнения ЛЖ не обладали предикторной значимостью в отношении неблагоприятного исхода сепсиса. Единственным предиктором летальности был показатель, определяемый с помощью ТПТД, ИФС, значение которого < 5,8 мин–1 предсказывало летальный исход с чувствительностью 85,7 % и специфичностью 72,2 %.
Таблица 1. Показатели ЭхоКГ, ТПТД и фармакологические индексы в момент исследования
Table 1. Echocardiography and transpulmonary thermodilution indicators and pharmacological indices at the time of the study
| Показатели | Ме [P25–P75] | M ± σ |
|---|---|---|
| ЧСС, мин–1 | 101,2 [88,6–114,4] | 98,4 ± 19,2 |
| ИКДОЛЖ, мл/м2 | 54,9 [40,1–66,4] | 56,2 ± 23,1 |
| ИКСОЛЖ, мл/м2 | 26,7 [20,2–32,22] | 27,8 ± 11,4 |
| ФИЛЖ, % | 55 [50–55] | – |
| ИУОэхо, мл/м2 | 27,8 [21,3–39,4] | 28,7 ± 12,4 |
| СИэхо, л/мин/м2 | 2,7 [2,2–4,0] | 2,95 ± 1,2 |
| СИтптд, л/мин/м2 | 3,2 [2,25–3,7] | 3,1 ± 0,9 |
| ИУОтптд, мл/м2 | 33,6 [24,7–41,2] | 32,6 ± 10,7 |
| ИГКДО, мл/м2 | 567,7 [498–672] | – |
| ГФИС, % | 23,3 [18,1–30,0] | 23,8 ± 7,5 |
| ИФС, мин–1 | 6,1 [5,2–6,8] | 5,9 ± 1,9 |
| Индекс общего периферического сосудистого сопротивления, дин × с × см–5 | 2221 [1601–2568] | 2173 ± 824 |
| ИИ, у.е. | 0 [0–7] | – |
| ВИИ, у.е. | 21,5 [2–38] | – |
Таблица 2. Корреляции показателей ЭхоКГ и ТПТД между собой и с фармакологическими индексами
Table 2. Correlations of echocardiography and transpulmonary thermodilution indicators with each other and with pharmacological indices
| Пары показателей | rho (r) | 95% ДИ | p |
|---|---|---|---|
| CИэхо–СИтптд | 0,462 (0,443)* | 0,082–0,725 (0,057–0,713)* | 0,02 (0,027)* |
| ИУОэхо–ИУОтптд | 0,538 (0,534)* | 0,182–0,770 (0,176–0,767)* | 0,0055 (0,006)* |
| ИКДОЛЖ–ИГКДО | 0,506 | 0,139–0,751 | 0,010 |
| ИКСОЛЖ–ИГКДО | 0,408 | 0,015–0,691 | 0,043 |
| ФИЛЖ–ГФИС | 0,507 | 0,139–0,751 | 0,010 |
| ФИЛЖ–ИФС | 0,351 | –0,05–0,655 | 0,085 |
| CИэхо–ИИ | –0,353 | –0,656–0,049 | 0,084 |
| CИэхо–ВИИ | –0,366 | –0,665–0,034 | 0,072 |
| CИтптд–ИИ | –0,576 | –0,791–0,235 | 0,003 |
| CИтптд–ВИИ | –0,378 | –0,672–0,021 | 0,063 |
| ФИЛЖ–ИИ | –0,132 | –0,501–0,277 | 0,528 |
| ФИЛЖ–ВИИ | –0,210 | –0,559–0,202 | 0,314 |
| ГФИС–ИИ | –0,327 | –0,640–0,078 | 0,110 |
| ГФИС–ВИИ | –0,244 | –0,569–0,188 | 0,282 |
| ИФС–ИИ | –0,429 | –0,705–0,041 | 0,032 |
| ИФС–ВИИ | –0,153 | –0,517–0,258 | 0,466 |
* В скобках приведены значения, полученные при помощи корреляции Пирсона для пар показателей с нормальным распределением.
Таблица 3. Ассоциированность показателей ТПТД с уровнем ФИЛЖ < 50 %
Table 3. Association of transpulmonary thermodilution indicators with the left ventricular ejection fraction level < 50 %
| Показатели | ОШ | 95% ДИ | p |
|---|---|---|---|
| СИэхо | 0,6972 | 0,2915–1,6676 | 0,4176 |
| ИУОэхо | 0,9987 | 0,9218–1,0820 | 0,9747 |
| ИГКДО | 1,0033 | 0,9988–1,0078 | 0,1487 |
| ГФИС | 0,9052 | 0,7945–1,0314 | 0,1647 |
| ИФС | 0,6982 | 0,4205–1,1592 | 0,1649 |
Таблица 4. Ассоциированность показателей ЭхоКГ, ТПТД и фармакологических индексов с летальностью
Table 4. Association of echocardiography and transpulmonary thermodilution indicators and pharmacological indices with mortality
| Показатели | ОШ | 95% ДИ | p |
|---|---|---|---|
| ИКДОЛЖ | 1,0117 | 0,9741–1,0507 | 0,548 |
| ИКСОЛЖ | 1,0235 | 0,9482–1,1048 | 0,552 |
| ФИЛЖ | 0,9690 | 0,8982–1,0454 | 0,416 |
| ИУОэхо | 0,9987 | 0,9291–1,0736 | 0,972 |
| СИэхо | 0,5747 | 0,2438–1,3547 | 0,206 |
| СИтптд | 0,3465 | 0,1093–1,0983 | 0,072 |
| ИУОтптд | 0,9880 | 0,9085–1,0745 | 0,778 |
| ИГКДО | 1,0064 | 0,9996–1,0133 | 0,065 |
| ГФИС | 0,8944 | 0,7779–1,0285 | 0,118 |
| ИФС | 0,3361 | 0,1351–0,8363 | 0,019 |
| ИИ | 0,9735 | 0,8295–1,1424 | 0,742 |
| ВИИ | 0,9907 | 0,9703–1,0115 | 0,378 |
Рис. 1. Объемы ЛЖ у больных с ФИЛЖ ³ 50 % и ФИЛЖ < 50 %
Fig. 1. Left ventricular volumes in patients with the left ventricular ejection fraction ³ 50 % and the left ventricular ejection fraction < 50 %

Рис.2. Корреляция ФИЛЖ и СИэхо
Fig. 2. Correlation the left ventricular ejection fraction and cardiac index(echocardiography)
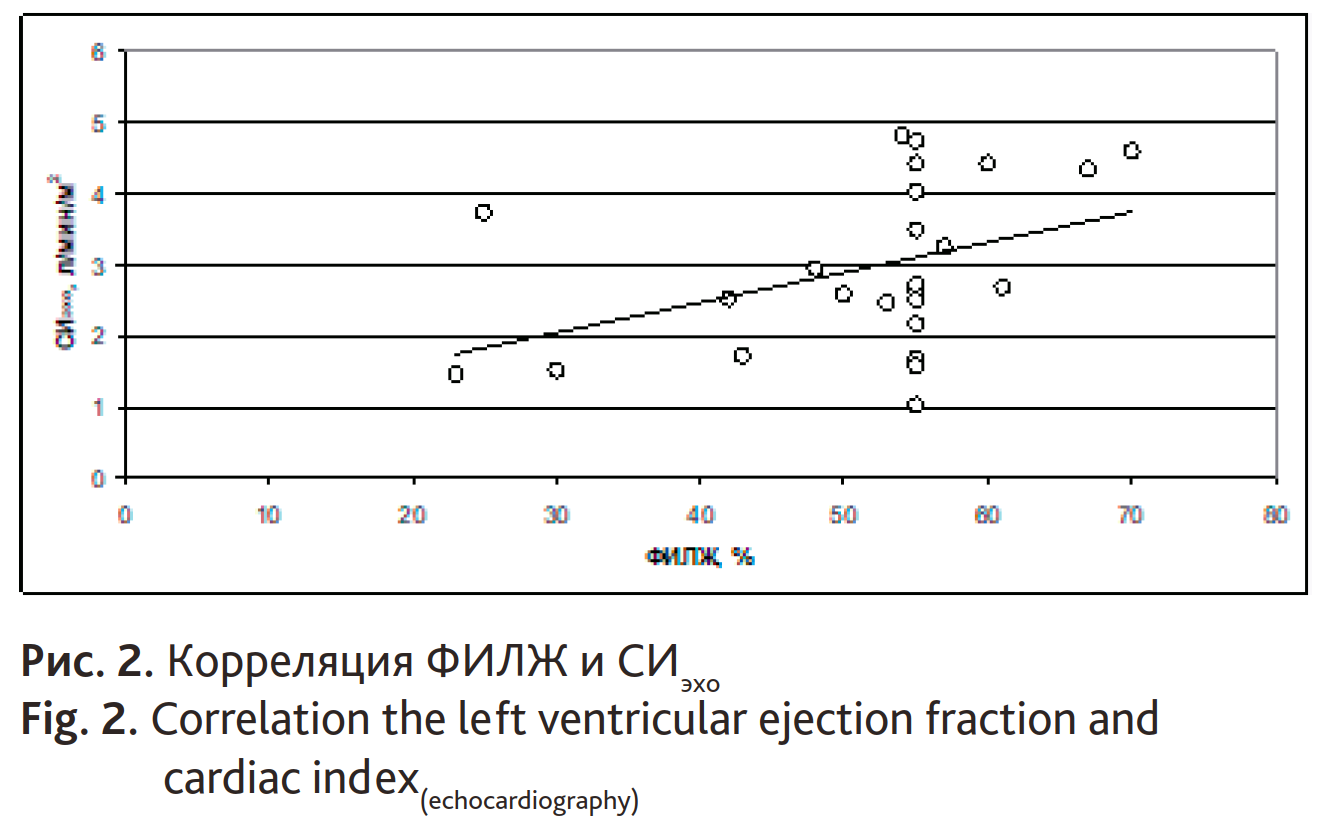
Рис. 3. ROC-кривая, отражающая разделительную способность ИФС в отношении летальности
Fig. 3. ROC-curve reflecting the separation capacity of the cardiac function index in relation to mortality

Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Информация о финансировании. Авторы заявляют об отсутствии внешнего финансирования при проведении исследования.
Вклад авторов. Тюрин И.Н., Раутбарт С.А., Ганиева И.И., Александровский А.А., Козлов И.А. — разработка концепции статьи, получение и анализ фактических данных, написание и редактирование текста статьи, проверка и утверждение текста статьи.